题目内容
完成并配平下列化学(或离子)方程式,标出(1)中电子转移的方向和数目.
(1) FeCl2+ KNO3+ KCl- FeCl3+ KCl+ NO+ H2O
(2) MnSO4+ K2S2O8+ - KMnO4+ K2SO4+ H2SO4
(3) SO32-+ MnO4-+ H+- Mn2++ SO42-+ H2O.
(1)
(2)
(3)
考点:氧化还原反应方程式的配平
专题:氧化还原反应专题
分析:(1)FeCl2→FeCl3,铁元素由+2价→+3价,化合价升高了1价;KNO3→NO,氮元素由+5价→+2价,化合价降低3价,化合价变化的最小公倍数为3,则氯化亚铁的计量数为3、硝酸钾的计量数为1,然后根据质量守恒定律配平;利用单线桥法表示出该反应中电子转移的方向和数目;
(2)MnSO4中的Mn元素化合价由+2价变为KMnO4中的+7,化合价升高5价;K2S2O8中S元素由+7降为硫酸根离子中的+6价,化合价至少降低2价,则化合价变化的最小公倍数为10,则MnSO4前配2,K2S2O8前配5,然后根据质量守恒定律判断未知物为水,再利用质量守恒定律配平即可;
(3)化合价变化为:SO32-→SO42-,硫元素由+4价→+6价,化合价升高了2价;MnO4-→Mn2+,锰元素由+7价→+2价,化合价降低了5价,所以其最小公倍数为10,亚硫酸根离子的系数为5,高锰酸根离子的系数为2,然后根据质量守恒定律配平.
(2)MnSO4中的Mn元素化合价由+2价变为KMnO4中的+7,化合价升高5价;K2S2O8中S元素由+7降为硫酸根离子中的+6价,化合价至少降低2价,则化合价变化的最小公倍数为10,则MnSO4前配2,K2S2O8前配5,然后根据质量守恒定律判断未知物为水,再利用质量守恒定律配平即可;
(3)化合价变化为:SO32-→SO42-,硫元素由+4价→+6价,化合价升高了2价;MnO4-→Mn2+,锰元素由+7价→+2价,化合价降低了5价,所以其最小公倍数为10,亚硫酸根离子的系数为5,高锰酸根离子的系数为2,然后根据质量守恒定律配平.
解答:
解:(1)反应方程式中元素的化合价变化为:FeCl2→FeCl3,铁元素由+2价→+3价,化合价升高了1价;
KNO3→NO,氮元素由+5价→+2价,化合价降低了3价,化合价变化的最小公倍数为3,所以氯化亚铁的计量数为3,硝酸钾的计量数为1,其它元素根据原子守恒配平,所以该方程式为:3FeCl2+1KNO3+4HCl=3FeCl3+1KCl+1NO↑+2H2O,用单线桥表示出电子转移的方向及数目为: ,
,
故答案为:3;1;4;3;1;1;2; ;
;
(2)MnSO4中的Mn元素化合价由+2升为KMnO4中的+7,化合价升高5价,
K2S2O8中S元素由+7降为硫酸根离子中的+6价,化合价至少降低(7-6)×2=2价,
则化合价变化的最小公倍数为10,所以MnSO4前配2,K2S2O8前配5,然后根据质量守恒定律判断未知物为水,再利用观察法配平,配平后的方程式为:2MnSO4+5K2S2O8+8H2O=2KMnO4+4K2SO4+8H2SO4,
故答案为:2;5;8;H2O;2;4;8;
(3)反应方程式中元素的化合价变化为 SO32-→SO42-,硫元素由+4价→+6价,化合价升高2价;
MnO4-→Mn2+,锰元素由+7价→+2价,化合价降低5价,所以其最小公倍数为10,故亚硫酸根离子的系数为5,高锰酸根离子的系数为2,其它元素根据原子守恒配平,所以该方程式为:5SO32-+2MnO4-+6H+=2Mn2++5SO42-+3H2O,
故答案为:5;2;6;2;5;3.
KNO3→NO,氮元素由+5价→+2价,化合价降低了3价,化合价变化的最小公倍数为3,所以氯化亚铁的计量数为3,硝酸钾的计量数为1,其它元素根据原子守恒配平,所以该方程式为:3FeCl2+1KNO3+4HCl=3FeCl3+1KCl+1NO↑+2H2O,用单线桥表示出电子转移的方向及数目为:
 ,
,故答案为:3;1;4;3;1;1;2;
 ;
;(2)MnSO4中的Mn元素化合价由+2升为KMnO4中的+7,化合价升高5价,
K2S2O8中S元素由+7降为硫酸根离子中的+6价,化合价至少降低(7-6)×2=2价,
则化合价变化的最小公倍数为10,所以MnSO4前配2,K2S2O8前配5,然后根据质量守恒定律判断未知物为水,再利用观察法配平,配平后的方程式为:2MnSO4+5K2S2O8+8H2O=2KMnO4+4K2SO4+8H2SO4,
故答案为:2;5;8;H2O;2;4;8;
(3)反应方程式中元素的化合价变化为 SO32-→SO42-,硫元素由+4价→+6价,化合价升高2价;
MnO4-→Mn2+,锰元素由+7价→+2价,化合价降低5价,所以其最小公倍数为10,故亚硫酸根离子的系数为5,高锰酸根离子的系数为2,其它元素根据原子守恒配平,所以该方程式为:5SO32-+2MnO4-+6H+=2Mn2++5SO42-+3H2O,
故答案为:5;2;6;2;5;3.
点评:本题考查了氧化还原反应的配平,题目难度中等,注意掌握氧化还原反应的实质及配平方法,能够利用单线桥、双线桥法分析氧化还原反应中电子转移的方向及数目.

练习册系列答案
 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案 新活力总动员暑系列答案
新活力总动员暑系列答案
相关题目
已知FeS2中铁元素的化合价为+2价,关于反应:4CuSO4+5FeS2+12H2O═7Cu2S+5FeSO4+12H2SO4的下列说法正确的是( )
| A、该反应的氧化剂只有CuSO4 | ||
| B、SO42-既不是氧化产物也不是还原产物 | ||
C、1 mol CuSO4还原了
| ||
| D、被还原的S和被氧化的S的质量比为7:3 |
下列说法中不正确的是.( )
| A、从1L 1mol/L的NaCl溶液中取出 10mL,其浓度仍是1mol/L |
| B、制成0.5 L 10 mol/L的盐酸,而要氯化氢气体112 L(标准状况) |
| C、0.5 L 2 mol/L BaCl2溶液中,Ba2+和Cl-总数为3×6.02×1023 |
| D、10g 98%的硫酸(密度为1.84 g/cm3)与10mL18.4mol/L硫酸的浓度是不同的 |
反应3X(g)+Y(g)?Z(g)+2W(g)在2L密闭容器中进行,5min后Y减少了0.1mol,则此反应的平均速率为( )
| A、v(X)=0.03 mol/(L?min) |
| B、v(Y)=0.02 mol/(L?min) |
| C、v(Z)=0.10 mol/(L?min) |
| D、v(w)=0.20 mol/(L?min) |
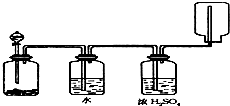 如图装置可以用来发生、洗涤、干燥、收集(不考虑尾气处理)气体,该装置可用于( )
如图装置可以用来发生、洗涤、干燥、收集(不考虑尾气处理)气体,该装置可用于( )| A、二氧化锰和双氧水反应生成氧气 |
| B、浓氨水和生石灰混合生成氨气 |
| C、Na2SO3和浓H2SO4混合生成SO2 |
| D、锌粒与稀盐酸混合生成H2 |