题目内容
4.25℃时,将氨水逐滴加入到稀硫酸中,当溶液的pH=7时,下列关系正确的是( )| A. | [NH4+]=[SO42-] | B. | [NH4+]>[SO42-] | ||
| C. | [NH4+]<[SO42-] | D. | [OH-]+[SO42-]=[H+]+[NH4+] |
分析 25℃时,将氨水逐滴加入到稀硫酸中,当溶液的pH=7时,c(H+)=c(OH-),依据溶液中的电荷守恒分析判断离子浓度大小;
解答 解:25℃时,将氨水逐滴加入到稀硫酸中,2NH3•H2O+H2SO4=(NH4)2SO4+2H2O,当溶液的pH=7时,c(H+)=c(OH-),依据溶液中的电荷守恒分析,电荷守恒为:c(H+)+c(NH4+)=c(OH-)+2c(SO42-),c(NH4+)=2c(SO42-),则[NH4+]>[SO42-],ACD错误,故选B.
点评 本题考查了电解质溶液中电荷守恒的分析应用,溶液呈中性c(H+)=c(OH-),题目较简单.

练习册系列答案
 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案
相关题目
15.金属能导电的原因是( )
| A. | 金属阳离子与自由电子间的作用较弱 | |
| B. | 金属在外加电场作用下可失去电子 | |
| C. | 金属阳离子在外加电场作用下可发生定向移动 | |
| D. | 自由电子在外加电场作用下可发生定向移动 |
12.在农业上,尿素CO(NH2)2、NH4NO3、NH4HCO3、(NH4)2CO3都可以做氮肥使用.在这四种物质中,氮的质量分数最高的是( )
| A. | 尿素CO(NH2)2 | B. | NH4NO3 | C. | NH4HCO3 | D. | (NH4)2CO3 |
19.下列有关氯气的叙述中错误的是( )
| A. | 氯气是一种有刺激性气味的气体 | B. | 氯气,液氯,氯水是同一种物质 | ||
| C. | 氯气能溶于水 | D. | 氯气是一种有毒气体 |
9.下列实验现象,与新制氯水中的某些成分(括号内物质)没有关系的是( )
| A. | 将NaHCO3固体加入新制氯水,有无色气泡(H+) | |
| B. | 使红色布条褪色(Cl2) | |
| C. | 氯水能够导电(ClO) | |
| D. | 滴加AgNO3溶液生成白色沉淀(Cl-) |
16.现有两瓶无标签的无色溶液,分别装有Na2CO3和NaHCO3,用下列试剂或方法能将两者区分的是( )
①Ca(OH)2 ②盐酸 ③CaCl2 ④NaOH ⑤加热.
①Ca(OH)2 ②盐酸 ③CaCl2 ④NaOH ⑤加热.
| A. | ①③ | B. | ①④ | C. | ②③ | D. | ②⑤ |
14.用已知物质的量浓度的NaOH溶液滴定未知物质的量浓度的盐酸,无论是酸往碱中滴还是碱往酸中滴,在其它操作正确规范的前提下,下列操作一定会使测定结果偏高的是( )
| A. | 酸式滴定管未用待测盐酸润洗 | |
| B. | 碱式滴定管未用标准碱液润洗 | |
| C. | 锥形瓶用蒸馏水洗净后未用待测液润洗 | |
| D. | 滴定前仰视读数,滴定后平视读数 |
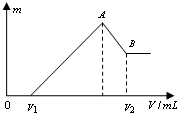 将0.1mol的镁、铝混合物溶于100mL 2mol/LH2SO4溶液中,然后再滴加1mol/L NaOH溶液.请回答:
将0.1mol的镁、铝混合物溶于100mL 2mol/LH2SO4溶液中,然后再滴加1mol/L NaOH溶液.请回答: