题目内容
15.如图为铜铁原电池示意图,心里有关说法正确的是( )
| A. | 电子由铁棒通过导线流向铜棒 | B. | 正极反应为Fe-2e-═Fe2+ | ||
| C. | 铜棒逐渐溶解 | D. | 该装置能将电能转化为化学能 |
分析 由图可知,该电池为铜铁原电池,Fe作负极,Cu作正极,发生Fe+2H+=Fe2++H2↑,电子由负极流向正极,以此来解答.
解答 解:A.铜铁原电池中,铜是电池的正极,Fe是负极,电子由Fe流向Cu,故A正确;
B.Fe作负极,Fe原子失去电子发生氧化反应,则负极的反应为Fe-2e-=Fe2+,故B错误;
C.铜铁原电池中,铜是电池的正极,Fe是负极,Fe逐渐溶解,故C错误;
D.该装置为铜锌原电池,是把化学能转化为电能的装置,故D错误;
故选A.
点评 本题考查原电池的工作原理,明确发生的原电池反应是解答本题的关键,题目较简单.

练习册系列答案
 手拉手全优练考卷系列答案
手拉手全优练考卷系列答案
相关题目
5.甲、乙、丙、丁是由H+、Na+、Al3+、Ba2+、OH-、Cl-、HCO3-离子中的两种组成,可以发生如图转化,下列说法不正确的是( )


| A. | 在甲中滴加丁可能发生反应:HCO3-+Ba2++OH-═BaCO3↓+H2O | |
| B. | 溶液丙中还可以大量共存的离子有:I-、NO3-、SO42- | |
| C. | 白色沉淀A可能溶解在溶液D中 | |
| D. | 甲为NaHCO3,乙为 AlCl3 |
6.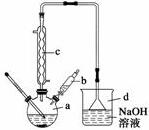 溴苯是一种常用的化工原料.实验室制备溴苯的实验步骤如下:
溴苯是一种常用的化工原料.实验室制备溴苯的实验步骤如下:
步骤1:在a中加入15mL苯和少量铁屑,再将b中4.0mL液溴慢慢加入到a中,充分反应.
步骤2:向a中加入10mL水,然后过滤除去未反应的铁屑.
步骤3:滤液依次用10mL水、8mL 10%的NaOH溶液,10mL水洗涤,分液得粗溴苯.
步骤4:向分出的粗溴苯中加入少量的无水氯化钙、静置、过滤即得粗产品.
(1)a中制备溴苯反应的化学方程式 +Br2$\stackrel{Fe}{→}$
+Br2$\stackrel{Fe}{→}$ +HBr.
+HBr.
(2)b中的液溴不能快速加入是为了防止因反应放热而使C6H6、Br2挥发(填化学式),影响产率.
(3)仪器c的作用是冷凝回流,d的作用是吸收HBr防污染防倒吸.
(4)步骤4得到的粗产品中还含有杂质苯.已知苯、溴苯的有关物理性质如上表,则要进一步提纯粗产品,还必须进行的实验操作名称是蒸馏.
 溴苯是一种常用的化工原料.实验室制备溴苯的实验步骤如下:
溴苯是一种常用的化工原料.实验室制备溴苯的实验步骤如下:步骤1:在a中加入15mL苯和少量铁屑,再将b中4.0mL液溴慢慢加入到a中,充分反应.
步骤2:向a中加入10mL水,然后过滤除去未反应的铁屑.
步骤3:滤液依次用10mL水、8mL 10%的NaOH溶液,10mL水洗涤,分液得粗溴苯.
步骤4:向分出的粗溴苯中加入少量的无水氯化钙、静置、过滤即得粗产品.
| 苯 | 溴 | 溴苯 | |
| 密度/gcm-3 | 0.88 | 3.10 | 1.50 |
| 沸点/℃ | 80 | 59 | 156 |
| 水中的溶解度 | 微溶 | 微溶 | 微溶 |
 +Br2$\stackrel{Fe}{→}$
+Br2$\stackrel{Fe}{→}$ +HBr.
+HBr.(2)b中的液溴不能快速加入是为了防止因反应放热而使C6H6、Br2挥发(填化学式),影响产率.
(3)仪器c的作用是冷凝回流,d的作用是吸收HBr防污染防倒吸.
(4)步骤4得到的粗产品中还含有杂质苯.已知苯、溴苯的有关物理性质如上表,则要进一步提纯粗产品,还必须进行的实验操作名称是蒸馏.
3.在过滤实验操作中,不需要用到的仪器是( )
| A. | 玻璃棒 | B. | 胶头滴管 | C. | 烧杯 | D. | 漏斗 |
10.用NA表示阿伏加德罗常数的值.下列判断正确的是( )
| A. | 1mol•L-1 K2SO4溶液中含有的SO42-离子数目为NA | |
| B. | 标准状况下,22.4LH2O含有的分子数目为NA | |
| C. | 常温常压下,22gCO2中含有的氧原子数目为NA | |
| D. | 1molMg变为Mg2+时失去的电子数目为NA |
20.用铂电极(惰性)电解下列溶液时,阴极和阳极的主要产物分别是H2和O2的是( )
| A. | 稀KOH溶液 | B. | HCl溶液 | C. | CuSO4溶液 | D. | NaCl溶液 |
7.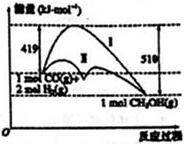 已知某反应过程在不同条件下的能量变化情况如图所示(改变的条件仅为催化剂),下列判断错误的是( )
已知某反应过程在不同条件下的能量变化情况如图所示(改变的条件仅为催化剂),下列判断错误的是( )
 已知某反应过程在不同条件下的能量变化情况如图所示(改变的条件仅为催化剂),下列判断错误的是( )
已知某反应过程在不同条件下的能量变化情况如图所示(改变的条件仅为催化剂),下列判断错误的是( )| A. | 反应物的总能量大于生成物的总能量 | |
| B. | 曲线Ⅰ和曲线Ⅱ相比较,曲线Ⅱ使用了催化剂 | |
| C. | 该反应可以表示为:CO(g)+2H2(g)?CH3OH(g)△=0.91KJ•mol-1 | |
| D. | 如果该反应生成液态CH3OH,则△H增大 |
4.下列各组物质发生的变化中,均属于化学变化的一组是( )
| A. | 鸡蛋清溶液中加入饱和(NH4)2SO4溶液生成白色沉淀;一束平行光照射蛋白质溶液时,从侧面可以看到光亮的通路 | |
| B. | 块状生石灰在空气中逐渐变成粉末;Na2CO3•10H2O在空气中逐渐变成粉末 | |
| C. | 木炭燃烧发光、发热;电灯发光、发热 | |
| D. | 石灰水中通入少量CO2后变浑浊;室温下的饱和石灰水加热后变浑浊 |
5.有a、b、c、d四个金属电极,有关的反应装置及部分反应现象如下:
由此可判断这四种金属的活动性顺序是( )
| 实验装置 | 部分实验现象 | 实验装置 | 部分实验现象 |
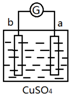 | a极质量减小, b极质量增加 | 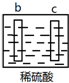 | b极有气体产生, c极无变化 |
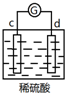 | d极溶解, c极有气体产生 | 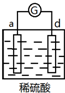 | 电流计指示在导线中电流从a极流向d极 |
| A. | d>a>b>c | B. | b>c>d>a | C. | a>b>c>d | D. | a>b>d>c |