题目内容
1.不属于氧化还原反应的是( )| A. | SiO2+CaO$\frac{\underline{\;高温\;}}{\;}$CaSiO3 | |
| B. | 2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$2MgO+C | |
| C. | N2+3H2$?_{△}^{催化剂}$2NH3 | |
| D. | C+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$2SO2↑+CO2↑+2H2O |
分析 氧化还原反应的实质为电子的转移,特征为化合价升降,则反应中存在化合价变化的反应为氧化还原反应,没有化合价变化的反应为非氧化还原反应,据此进行解答.
解答 解:A.SiO2+CaO$\frac{\underline{\;高温\;}}{\;}$CaSiO3,反应中没有元素化合价变化,不属于氧化还原反应,故A选;
B.2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$2MgO+C为置换反应,存在Mg、C化合价变化,属于氧化还原反应,故B不选;
C.N2+3H2$?_{△}^{催化剂}$2NH3为化合反应,存在N、H化合价变化,属于氧化还原反应,故C不选;
D.C+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$2SO2↑+CO2↑+2H2O中存在C、S元素的化合价变化,属于氧化还原反应,故D不选;
故选A.
点评 本题考查了氧化还原反应的判断,题目难度不大,明确氧化还原反应的实质、特征为解答关键,注意掌握常见反应类型与氧化还原反应的关系,试题有利于提高学生的灵活应用能力.

练习册系列答案
 口算能手系列答案
口算能手系列答案
相关题目
12.下列溶液中物质的量浓度为1mol•L-1的是( )
| A. | 将58.5 g NaCl溶解于1 L 水中 | |
| B. | 将22.4 L氨气溶于水配成1 L溶液 | |
| C. | 将1 L 10 mol•L-1的浓盐酸与9 L水混合 | |
| D. | 将10 g NaOH溶解在水中配成250 mL溶液 |
16.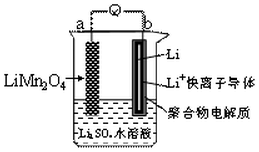 新能源汽车如(比亚迪秦、唐)相对传统汽车.有一系列的优点.如:环保、加速快(比亚迪唐0-100km/h加速时间仅需4.9秒).而新能源汽车一个核心部件为锂离子电池,如图是我国科学家报道的某种水溶液锂离子电池体系.下列叙述错误的是( )
新能源汽车如(比亚迪秦、唐)相对传统汽车.有一系列的优点.如:环保、加速快(比亚迪唐0-100km/h加速时间仅需4.9秒).而新能源汽车一个核心部件为锂离子电池,如图是我国科学家报道的某种水溶液锂离子电池体系.下列叙述错误的是( )
 新能源汽车如(比亚迪秦、唐)相对传统汽车.有一系列的优点.如:环保、加速快(比亚迪唐0-100km/h加速时间仅需4.9秒).而新能源汽车一个核心部件为锂离子电池,如图是我国科学家报道的某种水溶液锂离子电池体系.下列叙述错误的是( )
新能源汽车如(比亚迪秦、唐)相对传统汽车.有一系列的优点.如:环保、加速快(比亚迪唐0-100km/h加速时间仅需4.9秒).而新能源汽车一个核心部件为锂离子电池,如图是我国科学家报道的某种水溶液锂离子电池体系.下列叙述错误的是( )| A. | a为电池的正极 | |
| B. | 电池充电反应为LiMn2O4═Li1-xMn2O4+xLi | |
| C. | 放电时,a极锂的化合价发生变化 | |
| D. | 放电时,溶液中Li+从b向a迁移 |
6.下列有关热化学方程式的叙述正确的是( )
| A. | 已知2H2(g)+O2(g)═2H2O(g)△H=-483.6 kJ/mol,则氢气的燃烧热为241.8 kJ/mol | |
| B. | 已知C(石墨,s)=C(金刚石,s)△H>0,则金刚石比石墨稳定 | |
| C. | 已知2C(s)+2O2(g)═2CO2(g)△H12C(s)+O2(g)═2CO(g)△H2,则△H1>△H2 | |
| D. | 含20.0gNaOH的稀溶液与稀盐酸完全中和,放出28.7 kJ的热量,则该反应中和热的热方程式为:NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(l)△H=-57.4 kJ/mol |
13.下列离子方程式正确的是( )
| A. | 用醋酸除水垢:CaCO3+2H+═Ca2++H2O+CO2↑ | |
| B. | 用小苏打治疗胃酸过多:CO32-+2H+═CO2↑+H2O | |
| C. | 碳酸氢钠溶液与少量石灰水反应:2HCO3-+Ca2++2OH-═CaCO3↓+CO32-+2H2O | |
| D. | 向澄清石灰水中通入过量二氧化碳:Ca2++2OH-+CO2═CaCO3↓+H2O |
16.下列有关实验操作的说法正确的是( )
| A. | 蒸发操作时,应使混合物中的水分完全蒸干后,才能停止加热 | |
| B. | 检验氨气时,需用玻璃棒沾取湿润的红色石蕊试纸靠近导管口 | |
| C. | 用稀硝酸溶液洗涤并灼烧铂丝后,再进行焰色反应 | |
| D. | 用CCl4萃取溴水中的溴,分液时有机层从分液漏斗的上口倒出 |
17.在强酸性无色透明溶液中,下列各组离子能大量共存的是( )
| A. | Cu2+、K+、Cl-、NO3- | B. | Ag+、Na+、NO3-、Cl- | ||
| C. | Na+、Al3+、SO42-、Cl- | D. | Ba2+、NH4+、Cl-、CO32- |
 (写结构简式).
(写结构简式).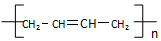 .
.