题目内容
铝土矿的主要成分是Al2O3,还含有Fe2O3、SiO2等杂质.从铝土矿中提取氧化铝的流程如图所示:

(1)操作1的名称是 ,所需要的主要玻璃仪器有: .
(2)试剂A是 ;(用化学式回答).
(3)溶液b与试剂B反应的离子方程式为 .
(4)请写出铝土矿加入足量NaOH溶液所发生的有关反应化学方程式: ,
(5)某同学认为可以向溶液a中通入的是过量的CO2,然后直接将得到的滤渣b煅烧后也可得到Al2O3,而且可以简化上述提取氧化铝的流程.你认为该同学的看法合理吗? (填“合理”或“不合理”)理由是: .(若认为合理该问题可以不回答)
(6)电解熔融的氧化铝可制备金属铝:2Al2O3
4Al+3O2↑.若在标准状况下生成2.24L的氧气,则该反应转移的电子数为 .

(1)操作1的名称是
(2)试剂A是
(3)溶液b与试剂B反应的离子方程式为
(4)请写出铝土矿加入足量NaOH溶液所发生的有关反应化学方程式:
(5)某同学认为可以向溶液a中通入的是过量的CO2,然后直接将得到的滤渣b煅烧后也可得到Al2O3,而且可以简化上述提取氧化铝的流程.你认为该同学的看法合理吗?
(6)电解熔融的氧化铝可制备金属铝:2Al2O3
| ||
考点:物质分离和提纯的方法和基本操作综合应用
专题:实验设计题
分析:SiO2和盐酸不反应,Fe2O3和氢氧化钠不反应而氧化铝能,该工艺流程原理为:铝土矿加入氢氧化钠,得到滤液a中含有偏铝酸根离子、硅酸根离子,沉淀a为氧化铁,a溶液加入过量为酸溶液,除去硅酸根离子,将偏铝酸根离子转化为铝离子,进入滤液b中,加过量氨水生成氢氧化铝沉淀,加热分解得氧化铝.电解熔融的氧化铝可制备金属铝,阳极生成氧气,阴极生成铝,据此分析和计算.
解答:
解:(1)分离不溶物和溶液的操作为过滤,铝土矿加入氢氧化钠,得到滤液a中含有偏铝酸根离子、硅酸根离子,沉淀a为氧化铁,故采用过滤的方法分离,过滤所用仪器为:铁架台、漏斗、玻璃棒、烧杯,故答案为:过滤;铁架台、玻璃棒、漏斗、烧杯;
(2)铝土矿与氢氧化钠反应生成偏铝酸钠,加入盐酸或硝酸等酸性溶液可除去硅酸根离子,故答案为:HCl;
(3)滤液b中含有铝离子、过量的盐酸,要使铝离子沉淀,需加入过量氨水,氨水和盐酸反应生成氯化铵,氨水和氯化铝反应生成氯化铵和氢氧化铝沉淀,反应的方程式为HCl+NH3?H2O=NH4Cl+H2O,AlCl3+3NH3?H2O=Al(OH)3↓+3NH4Cl,
故答案为:HCl+NH3?H2O=NH4Cl+H2O,AlCl3+3NH3?H2O=Al(OH)3↓+3NH4Cl;
(4)铝土矿的主要成分是Al2O3,还含有Fe2O3、SiO2等杂质,其中氧化铝、二氧化硅和氢氧化钠反应生成偏铝酸钠和硅酸钠,反应的方程式为:Al2O3+2NaOH═2NaAlO2+H2O、SiO2+2NaOH═Na2SiO3+H2O;
故答案为:Al2O3+2NaOH═2NaAlO2+H2O;SiO2+2NaOH═Na2SiO3+H2O;
(5)滤液a中含有偏铝酸根离子、硅酸根离子,向溶液a中通入的是过量的CO2,生成氢氧化铝沉淀和硅酸沉淀,然后直接将得到的滤渣b煅烧后得到氧化铝和二氧化硅,则Al2O3中含有SiO2杂质,故答案为:不合理;Al2O3中含有SiO2杂质;
(6)电解熔融的氧化铝可制备金属铝,阳极生成氧气,阴极生成铝,阳极反应为2O2--4e-=O2↑,
2O2--4e-=O2↑
4mol 22.4L
n 2.24L
n=
=0.4mol,故转移电子0.4NA,
故答案为:0.4NA.
(2)铝土矿与氢氧化钠反应生成偏铝酸钠,加入盐酸或硝酸等酸性溶液可除去硅酸根离子,故答案为:HCl;
(3)滤液b中含有铝离子、过量的盐酸,要使铝离子沉淀,需加入过量氨水,氨水和盐酸反应生成氯化铵,氨水和氯化铝反应生成氯化铵和氢氧化铝沉淀,反应的方程式为HCl+NH3?H2O=NH4Cl+H2O,AlCl3+3NH3?H2O=Al(OH)3↓+3NH4Cl,
故答案为:HCl+NH3?H2O=NH4Cl+H2O,AlCl3+3NH3?H2O=Al(OH)3↓+3NH4Cl;
(4)铝土矿的主要成分是Al2O3,还含有Fe2O3、SiO2等杂质,其中氧化铝、二氧化硅和氢氧化钠反应生成偏铝酸钠和硅酸钠,反应的方程式为:Al2O3+2NaOH═2NaAlO2+H2O、SiO2+2NaOH═Na2SiO3+H2O;
故答案为:Al2O3+2NaOH═2NaAlO2+H2O;SiO2+2NaOH═Na2SiO3+H2O;
(5)滤液a中含有偏铝酸根离子、硅酸根离子,向溶液a中通入的是过量的CO2,生成氢氧化铝沉淀和硅酸沉淀,然后直接将得到的滤渣b煅烧后得到氧化铝和二氧化硅,则Al2O3中含有SiO2杂质,故答案为:不合理;Al2O3中含有SiO2杂质;
(6)电解熔融的氧化铝可制备金属铝,阳极生成氧气,阴极生成铝,阳极反应为2O2--4e-=O2↑,
2O2--4e-=O2↑
4mol 22.4L
n 2.24L
n=
| 4mol×2.24L |
| 22.4L |
故答案为:0.4NA.
点评:本题考查较为综合,涉及物质的制备方案的设计与评价,注意把握制备原理的比较,把握物质的性质以及相关反应方程式的书写,难度中等.

练习册系列答案
相关题目
在化学变化中,原子结构中可能发生改变的是( )
| A、质子数 | B、中子数 |
| C、原子的核外电子数 | D、原子核 |
下列化学用语中,正确的是( )
A、Mg原子结构示意图  | ||||
| B、两个硫酸根离子:SO42- | ||||
C、质子数为6、中子数为8的碳原子:
| ||||
| D、三个氧原子:3O3 |
某同学设计如下实验测量m g铜银合金样品中铜的质量分数.
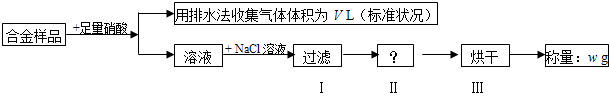
下列说法中不正确的是( )

下列说法中不正确的是( )
| A、收集到的V L气体全为 NO | ||
| B、过滤用到的玻璃仪器是:烧杯、漏斗、玻璃棒 | ||
| C、操作Ⅱ应是洗涤 | ||
D、铜的质量分数为:
|
工业上用铝土矿(主要成分为Al2O3,含Fe2O3杂质)为原料冶炼铝的工艺流程如下: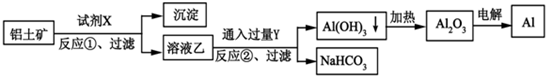
下列叙述正确的是( )

下列叙述正确的是( )
| A、试剂X可以是氢氧化钠溶液,也可以是盐酸 |
| B、反应①过滤后所得沉淀为氢氧化铁 |
| C、反应②通入的过量Y是CO2气体 |
| D、图中所示的转化反应①②都是氧化还原反应 |