题目内容
12.现有A、B、C、D 4种元素,前3种元素的离子都和氖原子具有相同的核外电子排布.A元素的非金属性最强;B的氢化物分子式为H2B,C单质燃烧时火焰为黄色.D的原子核中没有中子.(1)根据以上条件,推断A、B、C、D的元素名称:
A.氟,B.氧,
C.钠,D.氢.
(2)用电子式表示C与A相互结合成的化合物,指出其化合物的类型及化学键类型:
C+A:电子式
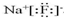 ,
,化合物类型:离子化合物,
化学键类型:离子键.
(3)写出C与B所形成的化合物与D和B所形成的化合物反应的离子方程式2Na2O2+2H2O=4Na++4OH-+O2↑或Na2O+H2O=2Na++2OH-
(4)写出下列粒子的结构示意图K
 O2-
O2-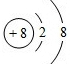 .
.
分析 A元素的非金属性最强,应为F元素;B的氢化物分子式为H2B,且元素的离子和氖原子具有相同的核外电子排布,应为O元素,C单质燃烧时火焰为黄色,为Na元素,D的原子核中没有中子,为H元素,结合对应单质、化合物的性质解答该题.
解答 解:(1)由上述分析可知,A为氟元素,B为氧元素,C为钠,D为氢元素,故答案为:氟;氧;钠;氢;
(2)C与A形成的化合物为NaF,电子式为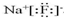 ,属于离子化合物,含有离子键,故答案为:
,属于离子化合物,含有离子键,故答案为: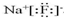 ,离子化合物,离子键;
,离子化合物,离子键;
(3)C与B所形成的化合物为Na2O2或Na2O,D和B所形成的化合物为H2O,二者反应的离子方程式为为2Na2O2+2H2O=4Na++4OH-+O2↑或Na2O+H2O=2Na++2OH-,故答案为:2Na2O2+2H2O=4Na++4OH-+O2↑或Na2O+H2O=2Na++2OH-;
(4)K原子核外有4个电子层,最外层电子数为1,原子结构示意图为 ,核外有2个电子层,最外层电子数为8,结构示意图为
,核外有2个电子层,最外层电子数为8,结构示意图为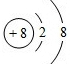 ,
,
故答案为: ;
;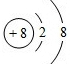 .
.
点评 本题考查结构性质位置关系应用,为高频考点,推断元素是解题关键,侧重对化学用语的考查,注意理解掌握用电子式表示化学键或物质的形成.

练习册系列答案
相关题目
9.X、Y、Z、W是四种原子序数依次增大的短周期元素.已知:X与W位于同一主族,且W的原子序数是X的2倍,Z是同周期中简单离子半径最小的元素,Y的原子序数比Z小l.下列说法不正确的是( )
| A. | Y、Z着火时均可用泡沫灭火器进行灭火 | |
| B. | 最高价氧化物对应水化物的碱性:Y>Z | |
| C. | Y、Z、W的简单离子都能促进水的电离 | |
| D. | 原子半径由小到大的顺序:X<W<Z<Y |
3.下列实验设计所得结论不可靠的是( )
| A. | 将电石与水反应产生的气体先通入CuSO4溶液再通入酸性KMnO4溶液中,溶液褪色说明有乙炔生成 | |
| B. | 某钾盐溶于盐酸,产生能使澄清石灰水变浑浊的无色气体,说明该钾盐是K2CO3或K2SO3 | |
| C. | 将浓硫酸和乙醇溶液共热产生的气体干燥后通入溴的四氯化碳溶液,溶液褪色,说明有乙烯生成 | |
| D. | 将苯、液溴、铁粉混合物反应产生的气体通入到AgNO3溶液中有淡黄色沉淀产生,不能说明有HBr生成 |
20.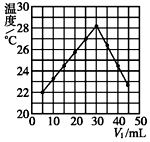 将V1 mL 1.0mol•L-1 HCl溶液和V2 mL未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如图所示(实验中始终保持V1+V2=50,溶液混前温度为21℃).下列叙述正确的是( )
将V1 mL 1.0mol•L-1 HCl溶液和V2 mL未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如图所示(实验中始终保持V1+V2=50,溶液混前温度为21℃).下列叙述正确的是( )
 将V1 mL 1.0mol•L-1 HCl溶液和V2 mL未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如图所示(实验中始终保持V1+V2=50,溶液混前温度为21℃).下列叙述正确的是( )
将V1 mL 1.0mol•L-1 HCl溶液和V2 mL未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如图所示(实验中始终保持V1+V2=50,溶液混前温度为21℃).下列叙述正确的是( )| A. | 该实验表明所有化学反应化学能只转化为热能 | |
| B. | NaOH溶液的浓度为1.0mol•L-1 | |
| C. | 该实验提供的数据能粗略计算出中和热 | |
| D. | 该实验可分多次把NaOH溶液倒入盛有盐酸的小烧杯中 |
7.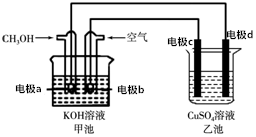 用该装置进行粗铜精炼,粗铜中一般含有锌、铁、银、金等杂质(此题中不考虑其他杂质)在如图所示的装置中,接通电路一段时间后,其中一个电极质量增加了3.2g,在此过程中,下列说法正确的是( )
用该装置进行粗铜精炼,粗铜中一般含有锌、铁、银、金等杂质(此题中不考虑其他杂质)在如图所示的装置中,接通电路一段时间后,其中一个电极质量增加了3.2g,在此过程中,下列说法正确的是( )
 用该装置进行粗铜精炼,粗铜中一般含有锌、铁、银、金等杂质(此题中不考虑其他杂质)在如图所示的装置中,接通电路一段时间后,其中一个电极质量增加了3.2g,在此过程中,下列说法正确的是( )
用该装置进行粗铜精炼,粗铜中一般含有锌、铁、银、金等杂质(此题中不考虑其他杂质)在如图所示的装置中,接通电路一段时间后,其中一个电极质量增加了3.2g,在此过程中,下列说法正确的是( )| A. | 甲池化学能转化为电能,工作时OH-由a→b定向移动 | |
| B. | 通电时,整个电路中电流方向为b→c,d→a | |
| C. | 乙池中CuSO4溶液的浓度不变 | |
| D. | 电极d是纯铜,此过程中电子转移0.05mol |
17.下列说法正确的是( )
| A. | Na与H2O的反应是熵增的放热反应,该反应能自发进行 | |
| B. | 镀锌制品镀层破损后,该铁制品比受损前更容易生锈 | |
| C. | 水中加入少量氯化铁固体,溶液中水的电离平衡会向右移动 | |
| D. | pH=3的盐酸与pH=10的某碱溶液等体积混合溶液呈碱性,说明该碱为强碱 |
4.如果你家里的食用菜油混有水分,你将采用下列何种方法分离( )
| A. | 过滤 | B. | 蒸馏 | C. | 分液 | D. | 萃取 |
1.某芳香族化合物的分子式为C7H6Cl2,该有机物的可能结构有(不考虑立体异构)( )
| A. | 9种 | B. | 10种 | C. | 11种 | D. | 12种 |
2.吗替麦考酚酯主要用于预防同种异体的器官排斥反应,其结构简式如图所示.下列说法正确的是( )


| A. | 吗替麦考酚酯的分子式为C23H30O7N | |
| B. | 吗替麦考酚酯可发生加成、取代、消去反应 | |
| C. | 吗替麦考酚酯分子中所有碳原子一定处于同一平面 | |
| D. | 1mol吗替麦考酚酯与NaOH溶液充分反应最多消耗3mol NaOH反应 |