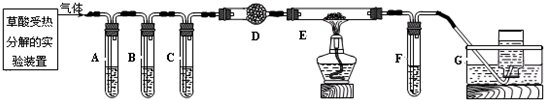
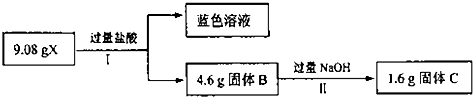
题目内容
 铝镁合金已成为轮船制造、化工生产等行业的重要材料.研究性学习小组的同学,为测定某不同品牌铝镁合金(不含其它元素)中镁的质量分数,设计下列两种不同实验方案进行探究.填写下列空白.
铝镁合金已成为轮船制造、化工生产等行业的重要材料.研究性学习小组的同学,为测定某不同品牌铝镁合金(不含其它元素)中镁的质量分数,设计下列两种不同实验方案进行探究.填写下列空白.[探究一]实验方案:铝镁合金
| 盐酸 |
实验装置如右图,问题讨论:
(1)反应完毕,每间隔1分钟读取气体体积,气体体积逐渐减小,直至不变.气体体积减小的原因是
(2)为使测定结果尽可能精确,实验中应注意的问题除了检查装置的气密性、加入足量盐酸使合金完全溶解和按(1)操作外,请再写出两点:
①
②
(3)如果用分析天平准确称取0.51g镁铝合进行实验,测得生成气体体积为560mL(已折算成标况下体积),请计算合金中镁的质量分数.(请写出计算过程)
[探究二]实验方案:称量Bg另一品牌铝镁合金粉末.放在如右图所示装置的惰性电热板上,通电使其充分灼烧.
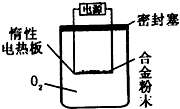
问题讨论:
(1)欲计算Mg的质量分数,该实验中还需测定的数据是
(2)用本方案进行实验时,装置中至少要充入O2的物质的量
[实验拓展]研究小组对某无色透明的溶液进行实验,发现该溶液跟铝反应时放出H2,试判断下列离子:Mg2+、Cu2+、Ba2+、H+、Ag+、SO42-、HCO3-、OH-、NO3-,在下列两种情况下,可能存在于此溶液中的是:
①当与铝反应后生成Al3+时,原溶液可能大量存在的离子
②当与铝反应后生成[Al(OH)4]-时,原溶液可能大量存在的离子是
考点:探究物质的组成或测量物质的含量
专题:实验探究和数据处理题
分析:[探究一](1)活泼金属与酸的反应是放热反应,故气体体积减小的原因是反应放热,气体温度较高,温度降低时,气体体积减小;
(2)①要使容器中的压强相等才能计量准确,即调整量气管C的高度,使C中液面与B液面相平;②排除认为的原因,即读数时保证视线与凹液面的最低点相平.
(3)560 mL即0.025mol,Mg~H2↑、Al~
H2↑,
24n(Mg)+27n(Al)=0.51、n(Mg)+
n(Al)=0.025;
解得:n(Al)=0.01mol
n(Mg)=0.01mol
m(Mg)=24n(Mg)=0.024g,合金中镁的质量分数为
×100%=47.1%.
[探究二](1)欲计算镁的质量分数,该实验中还需测定的一种数据是:完全反应后生成的固体的质量.
(2)如果合金全是铝,消耗氧气是最少的,关系式为Al~~~3/4O2,经计算得装置中至少要充入O2的物质的量为B/36mol.
[实验拓展](1)生成Al3+,证明体系中存在H+,能与H+共同存在的是Ba2+,Cu2+,Mg2+,H+,SO42-,NO3-,溶液无色,排除Cu2+
若存在NO3-,则不与Al反应产生H+,产生NO或者NO2,故而NO3-不存在,余下的Ba2+和SO42-不能同时存在
故而体系中存在Mg2+,H+,SO42-,无论哪种情况Ag+均不能存在,Ag2SO4和AgCl均溶解度小;
(2)生成AlO2-,证明体系含OH-
2Al+2OH-+2H2O=2AlO2-+3H2↑
含有OH-,则不能含有Mg2+(否则Mg(OH)2沉淀),不能有H+,不能有Ag+,不能有Cu2+,不能有HCO3-
剩余为Ba2+,SO42-,SO32-,NO3-,OH-,溶液中必有阳离子,Ba2+,所以没有SO32-和SO42-,只剩下:Ba2+,NO3-,OH-;
(2)①要使容器中的压强相等才能计量准确,即调整量气管C的高度,使C中液面与B液面相平;②排除认为的原因,即读数时保证视线与凹液面的最低点相平.
(3)560 mL即0.025mol,Mg~H2↑、Al~
| 3 |
| 2 |
24n(Mg)+27n(Al)=0.51、n(Mg)+
| 3 |
| 2 |
解得:n(Al)=0.01mol
n(Mg)=0.01mol
m(Mg)=24n(Mg)=0.024g,合金中镁的质量分数为
| 0.024g |
| 0.51g |
[探究二](1)欲计算镁的质量分数,该实验中还需测定的一种数据是:完全反应后生成的固体的质量.
(2)如果合金全是铝,消耗氧气是最少的,关系式为Al~~~3/4O2,经计算得装置中至少要充入O2的物质的量为B/36mol.
[实验拓展](1)生成Al3+,证明体系中存在H+,能与H+共同存在的是Ba2+,Cu2+,Mg2+,H+,SO42-,NO3-,溶液无色,排除Cu2+
若存在NO3-,则不与Al反应产生H+,产生NO或者NO2,故而NO3-不存在,余下的Ba2+和SO42-不能同时存在
故而体系中存在Mg2+,H+,SO42-,无论哪种情况Ag+均不能存在,Ag2SO4和AgCl均溶解度小;
(2)生成AlO2-,证明体系含OH-
2Al+2OH-+2H2O=2AlO2-+3H2↑
含有OH-,则不能含有Mg2+(否则Mg(OH)2沉淀),不能有H+,不能有Ag+,不能有Cu2+,不能有HCO3-
剩余为Ba2+,SO42-,SO32-,NO3-,OH-,溶液中必有阳离子,Ba2+,所以没有SO32-和SO42-,只剩下:Ba2+,NO3-,OH-;
解答:
解:[探究一](1)活泼金属与酸的反应是放热反应,故气体体积减小的原因是反应放热,气体温度较高,温度降低时,气体体积减小;
故答案为:反应放热,气体温度较高,温度降低时,气体体积减小;
(2)①要使容器中的压强相等才能计量准确,即调整量气管C的高度,使C中液面与B液面相平;②排除认为的原因,即读数时保证视线与凹液面的最低点相平;
故答案为:调整量气管C的高度,使C中液面与B液面相平;读数时保证视线与凹液面的最低点相平
(3)560 mL即0.025mol,Mg~H2↑、Al~
H2↑,
24n(Mg)+27n(Al)=0.51、n(Mg)+3/2 n(Al)=0.025.解得n(Al)=0.01mol,n(Mg)=0.01mol.
m(Mg)=24n(Mg)=0.024(g).合金中镁的质量分数为0.024g/0.51g*100%=47.1%;
答:合金中镁的质量分数为47.1%;
[探究二]①欲计算镁的质量分数,欲计算Mg的质量分数,该实验中还需测定的数据是灼烧后固体的质量;
故答案为:灼烧后固体的质量;
(2)如果合金全是铝,消耗氧气是最少的,关系式为Al~
O2,经计算得装置中至少要充入O2的物质的量为
mol;
故答案为:
;
[实验拓展](1)生成Al3+,证明体系中存在H+
能与H+共同存在的是Ba2+,Cu2+,Mg2+,H+,SO42-,NO3-,溶液无色,排除Cu2+
若存在NO3-,则不与Al反应产生H+,产生NO或者NO2,故而NO3-不存在
余下的Ba2+和SO42-不能同时存在
故而体系中存在Mg2+,H+,SO42-,无论哪种情况Ag+均不能存在,Ag2SO4和AgCl均溶解度小;原溶液可能大量存在的离子Mg2+,H+,SO42-;
故答案为:Mg2+,H+,SO42-;
②生成AlO2-,证明体系含OH-
2Al+2OH-+2H2O=2AlO2-+3H2↑
含有OH-,则不能含有Mg2+(否则Mg(OH)2沉淀),不能有H+,不能有Ag+,不能有Cu2+,不能有HCO3-
剩余为Ba2+,SO42-,SO32-,NO3-,OH-;
溶液中必有阳离子,Ba2+,所以没有SO32-和SO42-,只剩下:Ba2+,NO3-,OH-;
故答案为:Ba2+、OH-、NO3-;
故答案为:反应放热,气体温度较高,温度降低时,气体体积减小;
(2)①要使容器中的压强相等才能计量准确,即调整量气管C的高度,使C中液面与B液面相平;②排除认为的原因,即读数时保证视线与凹液面的最低点相平;
故答案为:调整量气管C的高度,使C中液面与B液面相平;读数时保证视线与凹液面的最低点相平
(3)560 mL即0.025mol,Mg~H2↑、Al~
| 3 |
| 2 |
24n(Mg)+27n(Al)=0.51、n(Mg)+3/2 n(Al)=0.025.解得n(Al)=0.01mol,n(Mg)=0.01mol.
m(Mg)=24n(Mg)=0.024(g).合金中镁的质量分数为0.024g/0.51g*100%=47.1%;
答:合金中镁的质量分数为47.1%;
[探究二]①欲计算镁的质量分数,欲计算Mg的质量分数,该实验中还需测定的数据是灼烧后固体的质量;
故答案为:灼烧后固体的质量;
(2)如果合金全是铝,消耗氧气是最少的,关系式为Al~
| 3 |
| 4 |
| B |
| 36 |
故答案为:
| B |
| 36 |
[实验拓展](1)生成Al3+,证明体系中存在H+
能与H+共同存在的是Ba2+,Cu2+,Mg2+,H+,SO42-,NO3-,溶液无色,排除Cu2+
若存在NO3-,则不与Al反应产生H+,产生NO或者NO2,故而NO3-不存在
余下的Ba2+和SO42-不能同时存在
故而体系中存在Mg2+,H+,SO42-,无论哪种情况Ag+均不能存在,Ag2SO4和AgCl均溶解度小;原溶液可能大量存在的离子Mg2+,H+,SO42-;
故答案为:Mg2+,H+,SO42-;
②生成AlO2-,证明体系含OH-
2Al+2OH-+2H2O=2AlO2-+3H2↑
含有OH-,则不能含有Mg2+(否则Mg(OH)2沉淀),不能有H+,不能有Ag+,不能有Cu2+,不能有HCO3-
剩余为Ba2+,SO42-,SO32-,NO3-,OH-;
溶液中必有阳离子,Ba2+,所以没有SO32-和SO42-,只剩下:Ba2+,NO3-,OH-;
故答案为:Ba2+、OH-、NO3-;
点评:本题主要考查物质含量的测定、对实验原理与装置的理解、实验方案设计等,难度中等,理解实验原理是解题的关键,是对知识的综合考查,需要学生具有知识的基础与综合运用知识分析问题、解决问题的能力.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列水解离子方程式正确的是( )
| A、CH3COO-+H2O?CH3COOH+OH- |
| B、NH4++H2O?NH4OH+H+ |
| C、Fe3++H2O?Fe(OH)3+H+ |
| D、Al3++3HCO3-═Al(OH)3↓+3CO2↑ |
经测定某溶液中离子只有Na+、CH3COO-、H+、OH-四种,且离子浓度大小的排列顺序为:c(Na+)>c(CH3COO-)>c(OH-)>c(H+)其可能的情形是( )
| A、该溶液由pH=3的CH3COOH溶液与pH=11的NaOH溶液等体积混合而成 |
| B、该溶液由0.2 mol/L的CH3COOH溶液与0.1 mol/L的NaOH溶液等体积混合 |
| C、在上述溶液中加入适量CH3COOH,可能使溶液中离子浓度大小改变为:c(Na+ )>c(CH3COO-)>c(H+)>c(OH-) |
| D、该溶液由0.1 mol/L的CH3COOH溶液与等物质的量浓度等体积的NaOH溶液混合而成 |

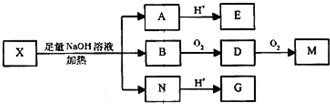
 反应制得有机物B(分子式为C9H8O4,遇FeCl3溶液不能显色),该反应的化学方程式是
反应制得有机物B(分子式为C9H8O4,遇FeCl3溶液不能显色),该反应的化学方程式是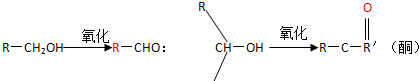
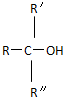 则很难被氧化(R、R+、R表示羟基).
则很难被氧化(R、R+、R表示羟基).
 乙二酸俗名草酸,下面是甲、乙两个化学学习小组的同学对草酸晶体(H2C2O4?xH2O)和草酸(H2C2O4)分别进行的探究性学习的过程,请你参与并协助他们完成相关学习任务.
乙二酸俗名草酸,下面是甲、乙两个化学学习小组的同学对草酸晶体(H2C2O4?xH2O)和草酸(H2C2O4)分别进行的探究性学习的过程,请你参与并协助他们完成相关学习任务.