题目内容
下列反应的离子方程式书写中,正确的是( )
| A、将氨水逐滴滴加到AlCl3溶液中:Al3++3OH-=Al(OH)3↓ |
| B、铜与稀硝酸反应:Cu+4H++NO3-=Cu2++NO↑+2H2O |
| C、硫酸与氢氧化钡在溶液中反应:Ba2++OH-+H++SO42-=BaSO4↓+H2O |
| D、用FeCl3溶液腐蚀铜箔制造的印刷电路板:2Fe3++Cu=2Fe2++Cu2+ |
考点:离子方程式的书写
专题:
分析:A.一水合氨在离子反应中保留化学式;
B.电子、电荷不守恒;
C.不符合离子的配比;
D.电子、电荷守恒.
B.电子、电荷不守恒;
C.不符合离子的配比;
D.电子、电荷守恒.
解答:
解:A.将氨水逐滴滴加到AlCl3溶液中的离子反应为Al3++3NH3.H2O=Al(OH)3↓+3NH4+,故A错误;
B.铜与稀硝酸反应的离子反应为3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O,故B错误;
C.硫酸与氢氧化钡在溶液中反应的离子反应为Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O,故C错误;
D.用FeCl3溶液腐蚀铜箔制造的印刷电路板的离子反应为2Fe3++Cu=2Fe2++Cu2+,故D正确;
故选D.
B.铜与稀硝酸反应的离子反应为3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O,故B错误;
C.硫酸与氢氧化钡在溶液中反应的离子反应为Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O,故C错误;
D.用FeCl3溶液腐蚀铜箔制造的印刷电路板的离子反应为2Fe3++Cu=2Fe2++Cu2+,故D正确;
故选D.
点评:本题考查离子反应方程式书写的正误判断,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重氧化还原反应、复分解反应的离子反应考查,题目难度不大.

练习册系列答案
 优生乐园系列答案
优生乐园系列答案
相关题目
某无色溶液中加入氢氧化铝,氢氧化铝迅速溶解,则该溶液中一定能够大量共存的离子组是( )
| A、K+、Na+、SO42-、Cl- |
| B、Na+、NH4+、SO42-、Cl- |
| C、Na+、K+、SO32-、NO3- |
| D、Na+、K+、MnO4-、Br- |
下列试剂中,能把NaOH溶液、稀硫酸、CaCl2溶液一次鉴别出来的是( )
| A、NaCl |
| B、稀盐酸 |
| C、NaNO3溶液 |
| D、Na2CO3溶液 |
经测定某溶液中离子只有Na+、CH3COO-、H+、OH-四种,且离子浓度大小的排列顺序为:c(Na+)>c(CH3COO-)>c(OH-)>c(H+)其可能的情形是( )
| A、该溶液由pH=3的CH3COOH溶液与pH=11的NaOH溶液等体积混合而成 |
| B、该溶液由0.2 mol/L的CH3COOH溶液与0.1 mol/L的NaOH溶液等体积混合 |
| C、在上述溶液中加入适量CH3COOH,可能使溶液中离子浓度大小改变为:c(Na+ )>c(CH3COO-)>c(H+)>c(OH-) |
| D、该溶液由0.1 mol/L的CH3COOH溶液与等物质的量浓度等体积的NaOH溶液混合而成 |
NaHCO3、Na2CO3?7H2O和Na2CO3?10H2O的混合物10g,溶于水配成1000mL溶液,取25mL溶液于锥形瓶中,甲基橙作指示剂用0.125mol?L-1的标准盐酸滴定,消耗盐酸20mL.若将10g这种混合物置于坩埚中加热到质量不变为止,剩余固体的质量为( )
| A、4.7g | B、5.0g |
| C、5.3g | D、5.5g |
对醋酸的电离平衡不产生影响的粒子是( )
A、H
| ||||||||
| B、HBr | ||||||||
C、 | ||||||||
D、 |
 反应制得有机物B(分子式为C9H8O4,遇FeCl3溶液不能显色),该反应的化学方程式是
反应制得有机物B(分子式为C9H8O4,遇FeCl3溶液不能显色),该反应的化学方程式是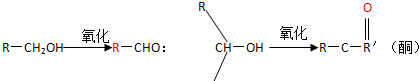
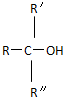 则很难被氧化(R、R+、R表示羟基).
则很难被氧化(R、R+、R表示羟基).