题目内容
对下列实验现象或操作解释错误的是( )
| 现象或操作 | 解释 | |||
| A | KI淀粉溶液中滴入氯水变蓝,再通入SO2,蓝色褪去 | SO2具有漂白性 | ||
| B | 苯酚中滴加浓溴水酸性明显增强 | 可能发生了取代反应 | ||
| C | 某溶液中加入硝酸酸化的氯化钡溶液,有白色沉淀生成 | 不能说明该溶液中一定含有SO
| ||
| D | 将SO2通入含HClO的溶液中,生成H2SO4, | HClO酸性比H2SO4强 |
| A、A | B、B | C、C | D、D |
考点:化学实验方案的评价
专题:
分析:A.KI淀粉溶液中滴入氯水变蓝,生成碘单质,再通入SO2,碘与二氧化硫发生氧化还原反应;
B.苯酚中滴加浓溴水,生成三溴苯酚沉淀和HBr;
C.白色沉淀为AgCl或硫酸钡;
D.将SO2通入含HClO的溶液中,发生氧化还原反应.
B.苯酚中滴加浓溴水,生成三溴苯酚沉淀和HBr;
C.白色沉淀为AgCl或硫酸钡;
D.将SO2通入含HClO的溶液中,发生氧化还原反应.
解答:
解:A.KI淀粉溶液中滴入氯水变蓝,生成碘单质,再通入SO2,碘与二氧化硫发生氧化还原反应,与二氧化硫的还原性有关,与漂白性无关,故A错误;
B.苯酚中滴加浓溴水,生成三溴苯酚沉淀和HBr,则发生取代反应后酸性增强,故B正确;
C.白色沉淀为AgCl或硫酸钡,则不能说明该溶液中一定含有硫酸根离子,可能含亚硫酸根离子,或银离子等,但银离子不能与硫酸根离子、亚硫酸根离子共存,故C错误;
D.将SO2通入含HClO的溶液中,发生氧化还原反应,不能利用该反应比较酸性,实际为硫酸酸性大于HClO的酸性,故D错误;
故选B.
B.苯酚中滴加浓溴水,生成三溴苯酚沉淀和HBr,则发生取代反应后酸性增强,故B正确;
C.白色沉淀为AgCl或硫酸钡,则不能说明该溶液中一定含有硫酸根离子,可能含亚硫酸根离子,或银离子等,但银离子不能与硫酸根离子、亚硫酸根离子共存,故C错误;
D.将SO2通入含HClO的溶液中,发生氧化还原反应,不能利用该反应比较酸性,实际为硫酸酸性大于HClO的酸性,故D错误;
故选B.
点评:本题考查化学实验方案的评价,为高频考点,涉及氧化还原反应、离子检验、有机反应等知识,把握物质的性质、反应原理等为解答的关键,侧重分析与应用能力的考查,选项D是易错点,注意实验的评价性分析,题目难度不大.

练习册系列答案
相关题目
设NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A、标准状况下,22.4LO3含有的氧原子数为2NA |
| B、7.1gCl2参加化学反应时,转移的电子数一定为0.2NA |
| C、常温常压下,0.2NA个NH3分子的质量为3.4g |
| D、1L0.2mol/L硫酸铁溶液中含有的SO42-离子数目为0.2NA |
下列实验设计或实验操作中,正确的是( )
A、 |
B、 |
C、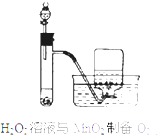 |
D、 |
下列操作能达到实验目的是( )
| A、将电石与水反应产生的气体通入酸性KMnO4溶液中,溶液褪色说明有乙炔生成 |
| B、将溴乙烷与NaOH的乙醇溶液共热产生的气体通入溴水中,溶液褪色说明有乙烯生成 |
| C、用苯、2mol/L硝酸和3mol/L硫酸制备硝基苯 |
| D、溴乙烷与氢氧化钠溶液共热后,加入硝酸银溶液检验Br- |
下列实验能获得成功的是( )
A、 实验室制取并检验乙烯 |
B、 实验室制取并检验乙炔 |
C、 实验室制取并检验氨气 |
D、 实验室制取溴苯 |
下列关于甲、乙、丙、丁四种仪器装置的有关用法中不合理的是( )


| A、甲装置:可用来证明硫的非金属性比硅强 |
| B、乙装置:橡皮管的作用是能使水顺利流下 |
| C、丙装置:用图示的方法能检查此装置的气密性 |
| D、丁装置:可在瓶中先装满水,气体由②口入,收集NO气体 |
 镁、铝、硅均为第三周期元素,按要求回答下列问题:
镁、铝、硅均为第三周期元素,按要求回答下列问题: 利用催化氧化反应将SO2转化为SO3是工业上生产硫酸的关键步骤.
利用催化氧化反应将SO2转化为SO3是工业上生产硫酸的关键步骤.