题目内容
6.下列说法正确是( )| A. | 向1mol的碳酸钾固体中缓缓滴加含1 mol溶质的稀盐酸会产生1mol的CO2气体 | |
| B. | 标准状况下,将64g 铜片投入到含 2 molH2SO4的浓硫酸中加热会产生22.4 L的SO2气体 | |
| C. | 标准状况下,用一充满氨气的干燥烧瓶做喷泉实验,当水充满整个烧瓶后(假设溶液不外溢),烧瓶内氨水的物质的量浓度为($\frac{1}{22.4}$)mol/L | |
| D. | 向含有1mol Ba(OH)2溶液中通入足量CO2气体产生1mol BaCO3白色沉淀 |
分析 A、碳酸钾和等量的盐酸之间反应生成的是碳酸氢钾,不会放二氧化碳;
B、金属铜和浓硫酸在解热下会反应,但是和稀硫酸不会发生反应;
C、根据物质的量浓度公式c=$\frac{n}{V}$来计算;
D、Ba(OH)2溶液中通入足量CO2气体得到的是碳酸氢钡溶液.
解答 解:A、1mol的碳酸钾固体中缓缓滴加含1mol溶质的稀盐酸之间反应生成的是碳酸氢钾,不会放二氧化碳,故A错误;
B、标准状况下,将64g铜片投入到含2mol H2SO4的浓硫酸中加热,会发生反应,但是随着反应的进行,硫酸变稀,金属铜和稀硫酸不会发生反应,所以产生SO2气体的体积会小于22.4L,故B错误;
C、假设充满氨气的干燥烧瓶的体积是V,氨气极易溶于水,得到一水合氨溶液,最后溶液的体积也是V,最后氨水的物质的量浓度c=$\frac{n}{V}$=$\frac{\frac{V}{22.4}}{V}$mol/L=$\frac{1}{22.4}$mol/L,故C正确;
D、Ba(OH)2溶液中通入足量CO2气体得到的是碳酸氢钡溶液,不会得到碳酸钡,故D错误.
故选C.
点评 本题涉及氨气以及浓硫酸化学性质的考查,注意B是易错点,物质的反应取决于所用反应物量的多少的反应要注意,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
3.下列物质中属于电解质并能导电的是( )
| A. | 液态氢氧化钾 | B. | 液态氯化氢 | C. | 氯化钠溶液 | D. | 碳棒 |
4.一定质量的Cu-Zn合金溶于足量的热浓硫酸中(忽略副反应),溶液所增加的质量与原合金质量之比为1:A,则原合金中Zn、Cu的质量之比为( )
| A. | 65:(A-65) | B. | 64:(A-65) | C. | 65:(A-64) | D. | 64:(A-64) |
14.粗盐提纯时不需用到的玻璃仪器是( )
| A. | 量筒 | B. | 玻璃棒 | C. | 三角漏斗 | D. | 容量瓶 |
1.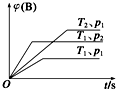 已知某可逆反应mA(g)+nB(g)?qC(g)△H在密闭容器中进行.如图表示在不同时刻t、温度T和压强p下B物质在混合气体中的体积分数φ(B)的变化情况.下列推断中正确的是( )
已知某可逆反应mA(g)+nB(g)?qC(g)△H在密闭容器中进行.如图表示在不同时刻t、温度T和压强p下B物质在混合气体中的体积分数φ(B)的变化情况.下列推断中正确的是( )
 已知某可逆反应mA(g)+nB(g)?qC(g)△H在密闭容器中进行.如图表示在不同时刻t、温度T和压强p下B物质在混合气体中的体积分数φ(B)的变化情况.下列推断中正确的是( )
已知某可逆反应mA(g)+nB(g)?qC(g)△H在密闭容器中进行.如图表示在不同时刻t、温度T和压强p下B物质在混合气体中的体积分数φ(B)的变化情况.下列推断中正确的是( )| A. | p1>p2,T1<T2,m+n>q,△H<0 | B. | p1<p2,T1>T2,m+n>q,△H<0 | ||
| C. | p1>p2,T1<T2,m+n<q,△H<0 | D. | p1<p2,T1>T2,m+n<q,△H>0 |
18.下列说法正确的是( )
| A. | 石油裂解、煤的气化、海水制镁等过程中都包含化学变化 | |
| B. | 通过化学变化可以实现235U与238U的相互转化 | |
| C. | 煤经气化、液化和干馏三个物理变化过程,可变为清洁能源 | |
| D. | 明矾和漂白粉常用于自来水的净化和杀菌消毒,两者的作用原理相同 |