题目内容
在实验室中进行合成氨工业的模拟实验,当反应进行一段时间,并建立相应的平衡以后,及时分离出氨并补充与起始原料比相同的氮气和氢气,以实现连续的生产过程。在1 L的密闭容器中,在一定条件下发生如下反应:N2(g)+3H2(g) ![]() 2NH3(g);ΔH<0
2NH3(g);ΔH<0

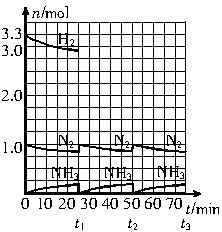
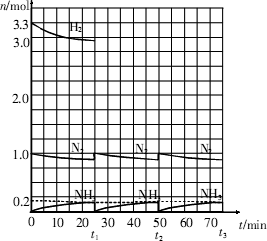
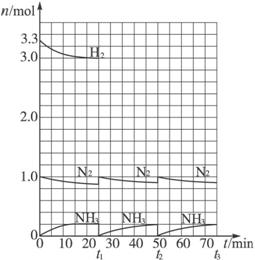
请根据图示回答下列问题:
(1)反应起始时,氮气与氢气的物质的量之比n(N2)∶n(H2)= _________∶_________。在15分钟时合成氨反应第一次达到平衡,其间以H2的浓度变化所表示的平均化学反应速率为_________________________。
(2)在t1时,曲线发生变化的原因是__________________、__________________。请计算氢气在t1起点时的坐标(_________,_________)以及在t2平衡时的坐标(_________,_________)。并在图中画出在t1—t2之间氢气的物质的量变化曲线。
(3)为达到图示中t2的平衡状态,在t1—t2之间需要采取的措施是_________。
a.扩大容器的体积
b.升高温度
c.降低温度
d.缩小容器的体积
(4)经历十次上述的循环过程,计算在t11达到平衡时,N2和H2的物质的量之比n(N2)∶n(H2)= _________∶_________,整个过程中N2和H2的总转化率之比α(N2)∶α(H2)= _________∶_________。
(5)根据以上计算结果,请你建议合成氨反应的最佳原料比是:n(N2)∶n(H2)=_________。
(1)1 3.3
0.02 mol·L-1·min-1
(2)分离氨气、补充物质的量之比为n(N2)∶n(H2)=1∶3.3的氮气和氢气 25 3.33 50 3.03
(3)a、b
(4)n(N2)∶n(H2) 3 11
α(N2)∶α(H2)=11∶10
(5)1∶3
图象

解析:(1)由图知n(N2)∶n(H2)=1∶3.3
![]()
(2)由图象的变化趋势知,分离NH3,并按比例补充反应混合气体,
坐标求算:N2 — 3H2
1 3
0.1 mol n(H2)
n(H2)=0.33 mol
所以t1时,n(H2)=3.0 mol+0.33 mol=3.33 mol,坐标(25,3.33)。
50 min平衡时,n(N2)减少0.1 mol,所以n(H2)减少0.3 mol,坐标(50,3.03)。
(3)从影响平衡的因素考虑,选ab。
(4)循环推算n(N2)∶n(H2)=3∶11,转化率=![]() =1∶3。
=1∶3。
(5)据(2)(4)数据,知最佳原料比1∶3。

 2NH3(g);ΔH<0
2NH3(g);ΔH<0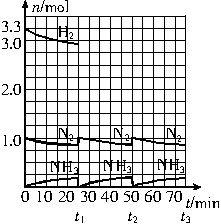
 2NH3(g);ΔH<0。请根据图示回答下列问题:
2NH3(g);ΔH<0。请根据图示回答下列问题: