题目内容
一定量的CH4燃烧后得到的产物是CO、CO2、H2O(g),此混合物的质量为49.6g,当其缓缓通过足量的无水CaCl2时气体质量减少25.2g,则混合气体中CO的质量为( )
| A、24.4g |
| B、13.2g |
| C、12.5g |
| D、11.2g |
考点:有关混合物反应的计算
专题:烃及其衍生物的燃烧规律
分析:无水氯化钙能够吸收水蒸气,气体质量减少25.2g为水蒸气质量,根据生成水的质量可以计算一氧化碳的质量,根据H原子守恒可计算CH4的物质的量,根据C原子守恒可计算CO、CO2的总的物质的量,令CO、CO2的物质的量分别为xmol、ymol,根据二者物质的量及质量列方程计算x、y的值,根据m=nM计算CO的质量.
解答:
解:无水CaCl2时CaCl2增重25.2克,则水的质量为25.2g,所以n(H2O)=
=1.4mol,
根据H原子守恒可计算CH4的物质的量为n(CH4)=
n(H2O)=
×1.4mol=0.7mol,
根据C原子守恒,可知CO和CO2的总的物质的量为0.7mol,
由于水的质量为25.2g,所以一氧化碳和二氧化碳的质量为:49.6g-25.2g=24.4g,
令CO、CO2的物质的量分别为xmol、ymol,则:
解得x=0.4,y=0.3,
所以混合气中CO的质量=0.4mol×28g/mol=11.2g,
故选D.
| 25.2g |
| 18g/mol |
根据H原子守恒可计算CH4的物质的量为n(CH4)=
| 1 |
| 2 |
| 1 |
| 2 |
根据C原子守恒,可知CO和CO2的总的物质的量为0.7mol,
由于水的质量为25.2g,所以一氧化碳和二氧化碳的质量为:49.6g-25.2g=24.4g,
令CO、CO2的物质的量分别为xmol、ymol,则:
|
解得x=0.4,y=0.3,
所以混合气中CO的质量=0.4mol×28g/mol=11.2g,
故选D.
点评:本题考查混合物计算,关键抓住化学反应前后C、H原子数目之比为1:4,难度中等.

练习册系列答案
 优百分课时互动系列答案
优百分课时互动系列答案 开心蛙状元作业系列答案
开心蛙状元作业系列答案
相关题目
某溶液中可能含有下列5中离子中的某几种:Na+、NH4+、Mg2+、Al3+、Cl-.为确认该溶液组成进行如下实验:①取20.0ml该溶液,加入25.0ml4.00mol/LNaOH溶液,有白色沉淀、无刺激气味气体生成.过滤、洗涤、干燥,得沉淀1.16g.再将滤液稀释至100ml,测得滤液中c(OH-)为0.20mol/L②另取20.0ml该溶液,加入足量的AgNO3溶液,生成白色沉淀11.48g由此可得出关于原溶液组成的正确结论是( )
| A、一定含Mg2+、Al3+、Cl-,不含Na+、NH4+ |
| B、一定含Na+、Mg2+、Cl-,不含NH4+,可能含有Al3+ |
| C、c(Cl-)为4.0mol/L,c(Al3+)为1.0mol/L |
| D、c(Mg2+)为1.0mol/L,c(Na+)为0.5mol/L |
38Sr(锶)与37Rb(铷)是同周期的相邻元素,下列有关锶的说法错误的是( )
| A、38Sr是第3周期ⅡA族元素 |
| B、Sr的离子半径比Ar的原子半径大 |
| C、Sr的碳酸盐受热会分解 |
| D、Sr的氧化物对应水化物碱性比Rb的氧化物对应水化物碱性弱 |
下列说法正确的是( )
| A、用酸性高锰酸钾即可鉴别苯酚溶液,2,4-己二烯和甲苯 |
B、按系统命名法化合物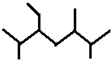 的名称为:2,5,6-三甲基-3-乙基庚烷 的名称为:2,5,6-三甲基-3-乙基庚烷 |
C、新型解热镇痛抗炎药贝诺酯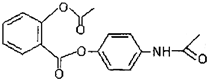 在酸性条件下完全水解可以得到3种有机物 在酸性条件下完全水解可以得到3种有机物 |
D、β-月桂烯的结构如图 ,一分子该物质与两分子溴发生加成反应的产物(只考虑位置异构)理论上最多有3种 ,一分子该物质与两分子溴发生加成反应的产物(只考虑位置异构)理论上最多有3种 |
 通常人们把拆开1mol某化学键所吸收的能量看成该化学键的键能.键能的大小可以衡量化学键的强弱,也可用于估算化学反应的反应热(△H),下表为一些常见化学键键能值.
通常人们把拆开1mol某化学键所吸收的能量看成该化学键的键能.键能的大小可以衡量化学键的强弱,也可用于估算化学反应的反应热(△H),下表为一些常见化学键键能值.