题目内容
4.莫尔盐[(NH4)2Fe(SO4)2•6H2O]常作氧化还原滴定法的基准物质,下列有关该盐溶液的比较,不正确的是( )| A. | c(SO42-)>c(NH4+)>c(Fe2+)>c(H+)>c(OH-) | B. | c(SO42-)=c(NH4+)>c(Fe2+)>c(H+)>c(OH-) | ||
| C. | 2c(SO42-)+c(OH-)=c(NH4+)+2c(Fe2+)+c(H+) | D. | c(NH4+)+c(NH3•H2O)=2c(Fe2+)+2c[Fe(OH)2] |
分析 该物质中NH4+、Fe2+都水解导致溶液呈酸性,且二者相互抑制水解,这两种离子水解程度较小,SO42-是强酸根离子,不水解;根据化学式知,溶液中c(NH4+)>c(Fe2+),任何电解质溶液中都存在电荷守恒和物料守恒,结合电荷守恒和物料守恒判断.
解答 解:A.SO42-是强酸根离子,不水解,NH4+、Fe2+都水解导致溶液呈酸性,且二者相互抑制水解,根据化学式知,溶液中c(NH4+)>c(Fe2+),弱离子水解程度较小,所以离子浓度大小顺序是c(SO42-)>c(NH4+)>c(Fe2+)>c(H+)>c(OH-),故A正确;
B.根据A知,离子浓度大小顺序是c(SO42-)>c(NH4+)>c(Fe2+)>c(H+)>c(OH-),故B错误;
C.根据电荷守恒得2c(SO42-)+c(OH-)=c(NH4+)+2c(Fe2+)+c(H+),故C正确;
D.根据物料守恒得c(NH4+)+c(NH3•H2O)=2c(Fe2+)+2c[Fe(OH)2],故D正确;
故选B.
点评 本题考查离子浓度大小比较,为高频考点,明确NH4+、Fe2+相互抑制水解是解本题关键,注意守恒思想的灵活运用,题目难度不大.

练习册系列答案
 同步奥数系列答案
同步奥数系列答案
相关题目
15.关于如图各实验装置的叙述中,不正确的是( )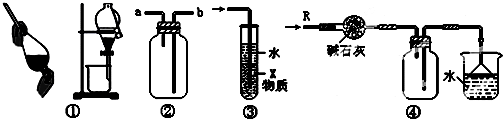

| A. | 装置①可用于分离乙醇和水的混合物 | |
| B. | 装置②可用于收集H2、NH3、CO2、Cl2、HCl、NO2等气体 | |
| C. | 装置③中X若为四氯化碳,可用于吸收氨气或氯化氢,并防止倒吸 | |
| D. | 装置④可用于干燥、收集氨气,并吸收多余的氨气 |
12.下列事实不能用平衡移动原理来解释的是( )
| A. | 打开啤酒瓶盖,产生大量气泡 | |
| B. | 稀释CH3COOH时,溶液中CH3COO-数目增多 | |
| C. | 工业合成氨常用500℃左右的温度 | |
| D. | 热的纯碱溶液的去污效果比冷的好 |
19.茶叶中铁元素的检验可经过以下四个步骤完成,各步骤中选用的实验用品不能都用到的是( )(Fe3+的检验滴加KSCN溶液)
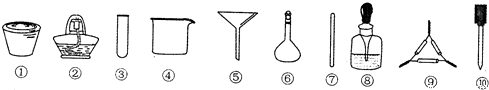

| A. | 将茶叶灼烧灰化,选用①、②和⑨ | |
| B. | 检验滤液中的Fe3+,选用③、⑧和⑩ | |
| C. | 用浓硝酸溶解茶叶灰并加蒸馏水稀释,选用④、⑥和⑦ | |
| D. | 过滤得到的滤液,选用④、⑤和⑦ |
9.化学与生活密切相关,下列说法正确的是( )
| A. | 凡含有食品添加剂的食物对人体健康均有害 | |
| B. | 苹果放在空气中久置变黄和纸张久置变黄原理相似 | |
| C. | 黄河入海口沙洲的形成与用卤水点豆腐,都体现了胶体聚沉的性质 | |
| D. | 制作航天服的聚酯纤维和用于光缆通信的光导纤维都是新型无机非金属材料 |
16.化学与生产、生活、环境等社会实际密切相关.下列叙述正确的是( )
| A. | “滴水石穿、绳锯木断”一定不涉及化学变化 | |
| B. | 明矾净水的原理和“84”消毒液消毒的原理不相同 | |
| C. | 充分开发利用天然纤维,停止使用各种化学合成材料 | |
| D. | 食品包装袋中常放入小袋的生石灰,目的是防止食品氧化变质 |
13.NA为阿伏加德罗常数,下列说法正确的是( )
| A. | NA个任何气体分子所占体积都约是22.4L | |
| B. | NA个H3O+含有电子数目为11NA | |
| C. | 0.5mol/L NaOH溶液中含有0.5NA个Na+ | |
| D. | NA个CO2和NO2的混合气体中氧原子数目为2NA |
