题目内容
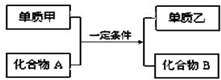 置换反应的通式可表示为如图:单质甲、乙和化合物A、B为中学常见物质,请回答下列问题:
置换反应的通式可表示为如图:单质甲、乙和化合物A、B为中学常见物质,请回答下列问题:(1)若A为两种元素形成常温下呈液态的化合物,化合物B的焰色反应呈黄色,则该反应的化学方程式为:
(2)若甲是一种金属单质,在高温条件下,本反应常用于焊接钢轨.则该反应的化学方程式为:
(3)若单质乙是黑色非金属固体单质,化合物B是一种白色金属氧化物,则该反应的化学方程式为:
考点:无机物的推断
专题:
分析:(1)若化合物A常温下呈液态,化合物B的焰色反应呈黄色,且为置换反应,则A为H2O,甲为Na,乙为H2,B为NaOH;
(2)若单质甲与化合物A发生的反应常用于野外焊接钢轨,则该反应为铝热反应,甲为铝,A为氧化铁,乙为铁,B为氧化铝;
(3)若单质乙是黑色非金属固体单质,化合物B是一种白色金属氧化物,应为Mg和CO2的反应.
(2)若单质甲与化合物A发生的反应常用于野外焊接钢轨,则该反应为铝热反应,甲为铝,A为氧化铁,乙为铁,B为氧化铝;
(3)若单质乙是黑色非金属固体单质,化合物B是一种白色金属氧化物,应为Mg和CO2的反应.
解答:
解:(1)若化合物A常温下呈液态,化合物B的焰色反应呈黄色,且为置换反应,则A为H2O,甲为Na,乙为H2,B为NaOH,反应化学方程式为2Na+2H2O=2NaOH+H2↑,
故答案为:2Na+2H2O=2NaOH+H2↑;
(2)若单质甲与化合物A发生的反应常用于野外焊接钢轨,则该反应为铝热反应,甲为铝,A为氧化铁,乙为铁,B为氧化铝,高温下,氧化铁和铝发生铝热反应生成铁和氧化铝,反应方程式为2Al+Fe2O3
Al2O3+2Fe,
故答案为:2Al+Fe2O3
Al2O3+2Fe;
(3)若单质乙是黑色非金属固体单质,化合物B是一种白色金属氧化物,应为Mg和CO2的反应,反应的方程式为2Mg+CO2
2MgO+C,
故答案为:2Mg+CO2
2MgO+C.
故答案为:2Na+2H2O=2NaOH+H2↑;
(2)若单质甲与化合物A发生的反应常用于野外焊接钢轨,则该反应为铝热反应,甲为铝,A为氧化铁,乙为铁,B为氧化铝,高温下,氧化铁和铝发生铝热反应生成铁和氧化铝,反应方程式为2Al+Fe2O3
| ||
故答案为:2Al+Fe2O3
| ||
(3)若单质乙是黑色非金属固体单质,化合物B是一种白色金属氧化物,应为Mg和CO2的反应,反应的方程式为2Mg+CO2
| ||
故答案为:2Mg+CO2
| ||
点评:本题以置换反应为载体考查了物质的推断,明确物质的性质是解本题关键,物质间的置换反应类型有:金属间的置换反应、非金属间的置换反应、金属和非金属之间的置换反应,难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
常温下,下列微粒在指定溶液中一定能大量共存的是( )
| A、在能使石蕊试液变红的溶液中:Ba2+、Cu2+、NO3-、Cl- |
| B、在pH=13的溶液中:K+、Mg2+、Cl-、SO32- |
| C、在乙醛水溶液中:K+、Na+、Cl-、Br2 |
| D、在由水电离c(H+)=1×10-12mol/L 的溶液中:Na+、K+、HCO3-、CH3COO- |
在下列给定条件的溶液中,一定能大量共存的离子组是( )
| A、澄清透明溶液:Al3+、Na+、SO42-、HCO3- | ||
B、常温下
| ||
| C、能使酚酞变红的溶液:K+、NH4+、Cl-、NO3- | ||
| D、无色溶液:K+、Na+、SO42-、Cu2+ |
在炼铁、制玻璃、制水泥三种工业生产中,都需要的原料是( )
| A、石灰石 | B、纯碱 | C、石英 | D、黏土 |
下列说法正确的是( )
| A、硅单质在电子工业上应用广泛,可作光导纤维 |
| B、糖类、油脂、蛋白质在一定条件下都能发生水解反应 |
| C、为了减少“白色污染”,我国规定商家不得提供塑料袋 |
| D、植物油和石油的裂化产品均能使酸性高锰酸钾溶液褪色 |
下列物质转化在给定条件下不能实现的是( )
①Si
SiO2
H2SiO3
②S
SO3
H2SO4
③C
CO2
Na2CO3
④MgCl2溶液
MgCl2?6H2O
Mg
⑤Na
Na2O2
NaOH.
①Si
| O2 |
| △ |
| H2O |
②S
| O2 |
| 点燃 |
| H2O |
③C
| SiO2 |
| 点燃 |
| NaOH |
④MgCl2溶液
| △ |
| 通电 |
| 熔化 |
⑤Na
| O2 |
| H2O |
| A、①②③ | B、①②④ |
| C、①②③④ | D、①②③④⑤ |
氨氧化制硝酸时.在吸收塔发生如下反应:3N〇2(g)+H2O(l)?2HNO3+NO(g),△H<0,为加快此反应的反应速率,下列措施不可行的是( )
| A、降低温度 |
| B、升高温度 |
| C、再加人NO2 |
| D、增大吸收塔中的压强 |
