题目内容
13.某混合溶液,含0.4mol HNO3,含0.2mol H2SO4,向其中加入3.84克铜,问生成NO多少mol?分析 根据反应3Cu+2NO3-+8H+=3Cu2++2NO+4H2O先判断离子的过量问题,然后根据不足量计算出生成NO的物质的量,最后根据V=nVm计算出生成NO在标准状况下的体积.
解答 解:某混合溶液,含0.4mol HNO3,含0.2mol H2SO4,则氢离子的物质的量为:n(H+)=0.4moL+2×0.2moL=0.8mol,
铜的物质的量为:$\frac{3.84g}{64g/mol}$=0.06mol,发生反应为:
3Cu+2NO3-+8H+=3Cu2++2NO+4H2O
3 2 8
0.06mol 0.4mol 0.8mol,
根据以上数据可知,氢离子、硝酸根离子过量,铜不足,
反应生成NO的物质的量为:n(NO)=$\frac{2}{3}$n(Cu)=0.06mol×$\frac{2}{3}$=0.04mol,
标准状况下0.04molNO的体积为:22.4L/mol×0.04mol=0.896L=896mL,
答:生成NO在标准状况下的体积为896mL.
点评 本题考查了化学方程式的计算,题目难度中等,正确判断过量情况为解答关键,注意掌握物质的量与摩尔质量、气体摩尔体积等之间的关系,试题培养了学生的化学计算能力.

练习册系列答案
 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案
相关题目
3.下列离子方程式或化学方程式与所述事实相符且正确的是( )
| A. | 向0.1 mol/L、pH=1的NaHA溶液中加入NaOH溶液:H++OH-═H2O | |
| B. | 以金属银为阳极电解饱和NaCl溶液:2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$ H2↑+Cl2↑+2OH- | |
| C. | 酸性条件下KIO3溶液与KI溶液发生反应生成I2:IO3-+5I-+3H2O═3I2+6OH- | |
| D. | NH4Al(SO4)2溶液中加入Ba(OH)2溶液使SO42-完全沉淀:Al3++2SO42-+2Ba2++4OH-═AlO2-+2BaSO4↓+2H2O |
1.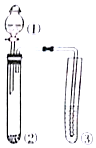 利用如图所示装置进行实验,仪器①②③中装下列试剂,③中现象描述正确的是( )
利用如图所示装置进行实验,仪器①②③中装下列试剂,③中现象描述正确的是( )
 利用如图所示装置进行实验,仪器①②③中装下列试剂,③中现象描述正确的是( )
利用如图所示装置进行实验,仪器①②③中装下列试剂,③中现象描述正确的是( )| 选项 | ① | ② | ③ | 试管③中现象 |
| A | 浓盐酸 | Na2SO3 | Ba(NO3)2溶液 | 无现象 |
| B | 稀盐酸 | 大理石 | 苯酚钠溶液 | 产生白色沉淀 |
| C | 稀盐酸 | 大理石 | CaCl2溶液 | 产生白色沉淀 |
| D | 浓硫酸 | 铜片 | KI-淀粉溶液 | 溶液变蓝 |
| A. | A | B. | B | C. | C | D. | D |
8.设NA表示阿伏加德罗常数,下列叙述不正确的是( )
| A. | 阿伏加德罗常数NA是0.012 kg 12C中所含的原子数 | |
| B. | 1 g氢气所含氢原子数目为NA | |
| C. | 标准状况下,22.4 L 乙醇所含的分子数目为NA | |
| D. | 1 L 1 mol•L-1 NaOH溶液中所含有的Na+离子数目为NA |
18.下列说法不正确的是( )
| A. | 同温、同压、同体积的12C18O和14N2具有的电子数相等 | |
| B. | 同温、同压、同体积的CO和NO含有的质子数相等 | |
| C. | 同温、同压、同体积的12C18O和14N2密度不相等 | |
| D. | 同温、同压、同体积的一氧化氮(14N18O)和一氧化碳(13C18O)气体含相同的分子数和原子数 |
5.下列实验装置正确且能完成实验目的是( )
| A. | 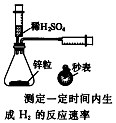 | B. | 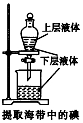 | C. |  | D. |  |
2.设阿伏加德罗常数的值为NA,则下列说法正确的是( )
| A. | 标准状况下,22.4 L乙烯含有的共用电子对数为5NA | |
| B. | 1 mol NaHSO4中的阳离子数为2NA | |
| C. | 通常状况下,1 mol NO和0.5 molO2 在密闭容器中混合,生成NO2分子数为NA | |
| D. | 制取漂白粉时,标准状况下22.4 LCl2 参加反应,转移电子数为NA |
3.下列实验的操作,通常情况下不能相互接触的是( )
| A. | 用胶头滴管向试管中滴加液体时,滴管尖端与试管内壁 | |
| B. | 过滤操作中,玻璃棒与三层滤纸 | |
| C. | 过滤操作中,漏斗下端管口与烧杯内壁 | |
| D. | 分液操作中,分液漏斗下端管口与烧杯内壁 |
 (一种常用的化妆品防霉剂),其生产过程如图(反应条件未全部注明)所示:
(一种常用的化妆品防霉剂),其生产过程如图(反应条件未全部注明)所示: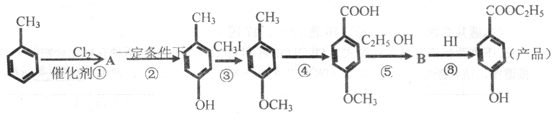
 ;
;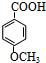 +C2H5OH$?_{△}^{浓硫酸}$
+C2H5OH$?_{△}^{浓硫酸}$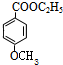 +H2O;
+H2O;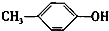 +CH3I→
+CH3I→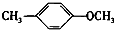 +HI.
+HI.