题目内容
20.下列除杂操作可行的是( )| A. | 通过浓硫酸除去HCl中的H2O | |
| B. | 通过灼热的CuO除去H2中的CO | |
| C. | 通过灼热的镁粉除去CO2中的N2 | |
| D. | 通过饱和碳酸氢钠溶液除去Cl2中的HCl |
分析 A、HCl是酸性气体;
B、氢气能和CuO发生氧化还原反应;
C、镁粉能和二氧化碳反应;
D、饱和碳酸氢钠溶液水解显弱碱性.
解答 解:A、HCl是酸性气体,无强还原性,能用浓硫酸干燥,故A正确;
B、氢气也能和CuO发生氧化还原反应:CuO+H2$\frac{\underline{\;△\;}}{\;}$Cu+H2O,故不能用氧化铜除去氢气中的CO,B错误;
C、镁粉也能和二氧化碳反应:Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$2MgO+C,故C错误;
D、饱和碳酸氢钠溶液水解显弱碱性,能吸收氯气,故不能用饱和碳酸钠溶液除去氯气中的HCl,故D错误.
故选A.
点评 物质的除杂是考试的重点,应根据杂质和主体物质的性质的不同点来分析,难度不大.

练习册系列答案
 每课必练系列答案
每课必练系列答案
相关题目
10.下列陈述正确并且有因果关系的是( )
| 选项 | 陈述Ⅰ | 陈述Ⅱ |
| A | SO2有漂白性 | SO2可使溴水褪色 |
| B | Cl2有漂白性 | Cl2能使品红溶液褪色 |
| C | 浓硫酸有脱水性 | 浓硫酸可用于干燥H2和CO |
| D | Fe3+有强氧化性 | FeCl3溶液可用于回收废旧电路板中的铜 |
| A. | A | B. | B | C. | C | D. | D |
11.将0.15mol Fe3O4完全溶解在足量稀硫酸中,然后加入K2Cr2O7溶液250mL,恰好使溶液中Fe2+全部氧化成Fe3+,Cr2O72-全部转化成Cr3+,则K2Cr2O7溶液的物质的量浓度是( )
| A. | 0.05mol/L | B. | 0.1mol/L | C. | 0.2mol/L | D. | 0.3mol/L |
8.下列变化是放热反应的是( )
①碳的燃烧 ②将胆矾加热变为白色粉末 ③浓硫酸稀释
④氯酸钾分解制氧气 ⑤生石灰与水反应生成熟石灰.
①碳的燃烧 ②将胆矾加热变为白色粉末 ③浓硫酸稀释
④氯酸钾分解制氧气 ⑤生石灰与水反应生成熟石灰.
| A. | ①③⑤ | B. | ②③ | C. | ①⑤ | D. | ②④ |
15.在一定条件下,Na2CO3溶液中存在水解平衡:CO32-+H2O?HCO3-+OH-.下列说法不正确的是( )
| A. | 通入CO2,溶液pH减小 | |
| B. | 加入少量NH4Cl固体,平衡向正反应方向移动 | |
| C. | 慢慢升高温度,$\frac{c(HC{O}_{3}^{-})}{c(C{O}_{3}^{2-})}$逐渐减小 | |
| D. | 加入NaOH 固体后冷却到室温,溶液的KW=c(OH-)•c(H+)不变 |
12.下列物质中,阳离子与阴离子的个数比等于2:1的是( )
| A. | Na2CO3溶液 | B. | H2S气体 | C. | NaHSO4固体 | D. | Na2O2固体 |
9.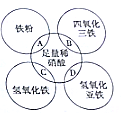 已知稀硝酸是强氧化性酸,还原产物一般为NO,如图两圆相交部分A、B、C、D分别表示两物质间的反应,下列各对应反应的离子方程式书写不正确的是( )
已知稀硝酸是强氧化性酸,还原产物一般为NO,如图两圆相交部分A、B、C、D分别表示两物质间的反应,下列各对应反应的离子方程式书写不正确的是( )
 已知稀硝酸是强氧化性酸,还原产物一般为NO,如图两圆相交部分A、B、C、D分别表示两物质间的反应,下列各对应反应的离子方程式书写不正确的是( )
已知稀硝酸是强氧化性酸,还原产物一般为NO,如图两圆相交部分A、B、C、D分别表示两物质间的反应,下列各对应反应的离子方程式书写不正确的是( )| A. | Fe+4H++NO3-═Fe3++NO↑+2H2O | |
| B. | Fe3O4+8H+═Fe2++2Fe3++4H2O | |
| C. | Fe(OH)3+3H+═Fe3++3H2O | |
| D. | 3Fe(OH)2+10H++NO3-═3Fe3++NO↑+8H2O |
16.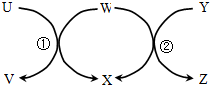 如图中U→Z六种物质在适当条件下能实现图示箭头方向一步转化,且反应①、②均为置换反应,满足条件的物质组是( )
如图中U→Z六种物质在适当条件下能实现图示箭头方向一步转化,且反应①、②均为置换反应,满足条件的物质组是( )
 如图中U→Z六种物质在适当条件下能实现图示箭头方向一步转化,且反应①、②均为置换反应,满足条件的物质组是( )
如图中U→Z六种物质在适当条件下能实现图示箭头方向一步转化,且反应①、②均为置换反应,满足条件的物质组是( )| 序号 | U | W | Y | X |
| ① | Na | H2O | Na2O2 | NaOH |
| ② | Fe | H2O | C | H2 |
| ③ | HBr | Cl2 | CH4 | HCl |
| ④ | CuCl2(aq) | Al | HCl(aq) | AlCl3(aq) |
| A. | ②④ | B. | ②③ | C. | ①②④ | D. | ①②③④ |