题目内容
20.天津港“8•12”特别重大火灾爆炸事故教训深刻.事故现场的装箱区有镁、钠、硫、氯酸钾、硝酸钾、硝酸铵、氰化钠、电石等多达上百种危化物.(1)硝酸铵受热分解爆炸:5NH4NO3═4N2↑+2HNO3+9H2O,1mol NH4NO3分解转移的电子的物质的量为3mol,氧化产物与还原产物的质量之比为5:3;
(2)储存电石的仓库不能使用水灭火,写出反应方程式CaC2+2H2O-→Ca(OH)2+C2H2↑;乙炔通入酸性KMnO4溶液被氧化为CO2气体,若KMnO4被还原为Mn2+,则该反应的离子方程式为C2H2+2MnO4-+6H+=2CO2↑+2Mn2++4H2O;
(3)为消除事故中心外泄氰化钠的毒性,主要采用碱性氯化法处理.原理如下:
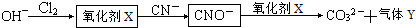
①写出氧化剂X的化学式ClO-(填离子符号),Y是N2(填化学式).
②(CN)2的性质与卤素单质很相似,且氧化性:F2>Cl2>Br2>(CN)2>I2.下列有关反应方程式不正确的是C(填序号).
A.(CN)2和NaOH溶液反应:(CN)2+2OH-═CN-+CNO-+H2O
B.MnO2和HCN反应:MnO2+4HCN═Mn(CN)2+(CN)2↑+2H2O
C.向KCN溶液中加入碘水:I2+2KCN=2KI+(CN)2.
分析 (1)该反应中N元素化合价由-3价、+5价变为0价,则氮气既是氧化产物也是还原产物,转移电子个数是15,根据转移电子守恒知,生成的氮气中有$\frac{5}{8}$的是氧化产物,有$\frac{3}{8}$的是还原产物,据此分析解答;
(2)碳化钙与水反应生成可燃性气体乙炔;高锰酸钾溶液能把乙炔氧化为二氧化碳,KMnO4被还原为Mn2+;
(3)氯气与氢氧根离子反应生成具有强氧化性的次氯酸根离子,ClO-把CN-氧化为CNO-,最后氧化为氮气和碳酸根离子,结合氧化还原反应原理分析.
解答 解:(1)该反应中N元素化合价由-3价、+5价变为0价,则氮气既是氧化产物也是还原产物,转移电子个数是15,则1mol NH4NO3分解转移的电子的物质的量为3mol;根据转移电子守恒知,生成的氮气中有$\frac{5}{8}$的是氧化产物,有$\frac{3}{8}$的是还原产物,所以氧化产物与还原产物的质量之比为$\frac{5}{8}$:$\frac{3}{8}$=5:3;
故答案为:3;5:3;
(2)碳化钙与水反应生成可燃性气体乙炔,其反应方程式为CaC2+2H2O-→Ca(OH)2+C2H2↑;高锰酸钾溶液能把乙炔氧化为二氧化碳,KMnO4被还原为Mn2+,其反应的离子方程式为:C2H2+2MnO4-+6H+=2CO2↑+2Mn2++4H2O;
故答案为:CaC2+2H2O-→Ca(OH)2+C2H2↑;C2H2+2MnO4-+6H+=2CO2↑+2Mn2++4H2O;
(3)氯气与氢氧根离子反应生成具有强氧化性的次氯酸根离子,ClO-把CN-氧化为CNO-,最后氧化为氮气和碳酸根离子,
①由分析可知,氧化剂X的化学式为ClO-,Y为N2;
故答案为:ClO-;N2;
②氰(CN)2的化学性质与卤素(X2)很相似,且氧化性:F2>Cl2>Br2>(CN)2>I2;
A.(CN)2和NaOH溶液反应可以类推氯气和氢氧化钠溶液的反应,所以反应的离子方程式为:(CN)2+2OH-═CN-+CNO-+H2O,故A正确;
B.MnO2和HCN反应可以类推二氧化锰和浓盐酸的反应,所以费用的化学方程式为:MnO2+4HCN $\frac{\underline{\;\;△\;\;}}{\;}$Mn(CN)2+(CN)2↑+2H2O,故B正确;
C.向KCN溶液中加入碘水,可以类推置换反应,(CN)2的氧化性比I2强:不能发生反应I2+2KCN═2KI+(CN)2,故C错误;
故答案为:C.
点评 本题考查氧化还原反应、元素化合物的性质,把握题干信息及知识迁移应用为解答的关键,侧重分析与计算的考查,题目难度中等.

| A. | 若样品为水溶液且只取一次有机物,检验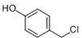 中官能团,应该先向其中加入 三氯化铁溶液检验酚羟基;再加入足量氢氧化钠溶液,加热,用稀硝酸酸化后,最后加入 硝酸银溶液检验氯原子 中官能团,应该先向其中加入 三氯化铁溶液检验酚羟基;再加入足量氢氧化钠溶液,加热,用稀硝酸酸化后,最后加入 硝酸银溶液检验氯原子 | |
| B. | 只检验 CH2=CH-CHO 中的碳碳双键不能用溴水,但是可以用溴的四氯化碳溶液 | |
| C. | 若样品为水溶液且只取一次有机物,检验 ClCH2COOH 中官能团,应该先加入足量氢 氧化钠溶液,加热,再用足量稀硝酸酸化后,加入硝酸银溶液检验氯原子;最后加入碳酸 氢钠溶液检验羧基 | |
| D. | 若样品为水溶液且只取一次有机物,检验邻羟基苯甲醇中的官能团,应该先加入紫色 石蕊试液检验酚羟基;再加入金属钠检验醇羟基 |
| A. | 等于7 | B. | 小于7 | C. | 大于7 | D. | 不能确定 |
| A. | 能使湿润的酚酞试液变红 | |
| B. | 能使湿润的红色石蕊试纸变蓝 | |
| C. | 氨气的水溶液呈中性 | |
| D. | 气体与蘸有浓盐酸的玻璃棒靠近产生大量白烟 |
| A. | 22.4 L O2中含有氧分子的个数为2NA | |
| B. | 24g Mg与足量氧气反应转移的电子数为2NA | |
| C. | 28g N2和CO的混合气体中含有的原子个数为4NA | |
| D. | 1 mol•L-1MgCl2溶液中含有氯离子个数为2NA |
| A. | 向苦卤(含K+、Mg2+、Br-等)中通入Cl2是为了提取溴 | |
| B. | 粗盐(含Ca2+、Mg2+、SO42-、泥沙等杂质)可采用除杂和重结晶等过程提纯 | |
| C. | 海带提碘只涉及物理变化,海水提镁涉及复分解反应 | |
| D. | 富集溴一般先用空气和水蒸气吹出单质溴,再用SO2将其还原吸收 |