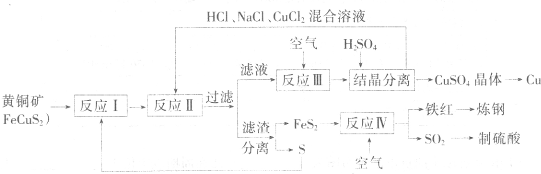
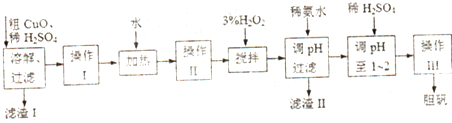
题目内容
已知Cu2+和Fe2+在pH为4—5的环境中不水解,而此种条件下,Fe3+几乎全部水解。双氧水(H2O2)是强氧化剂,在酸性条件下,它的还原产物为水。用粗氧化铜(含少量铁)制纯CuCl2溶液的过程如下:
①取50 mL稀盐酸,加入一定量粗氧化铜,加热、搅拌,充分反应后过滤,经测定溶液pH约为2;
②向滤液中加入双氧水搅拌;
③向滤液中加入过量的纯氧化铜、微热,充分搅拌,经测定溶液的pH约是5;
④过滤;
⑤浓缩溶液。
(1)操作②中的离子方程式:______________________________。
(2)操作④中过滤后滤渣的成分为__________________________。
(3)浓缩过程中溶液颜色的变化:__________________________。
(4)操作③中发生反应的离子方程式为______________________。
(1)H2O+2Fe2++2H+![]() 2Fe3++2H2O
2Fe3++2H2O
(2)Fe(OH)3、CuO
(3)由蓝色变绿色
(4)CuO+2H+![]() Cu2++H2O
Cu2++H2O

 天天练口算系列答案
天天练口算系列答案粗CuO是将工业废铜、废铜合金等高温焙烧而成的,杂质主要是铁的氧化物及泥沙。以粗CuO为原料制备胆矾的主要流程如下:
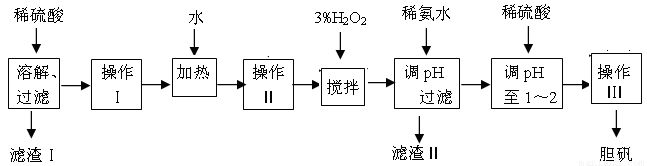
已知Fe3+、Fe2+ 、Cu2+转化为相应氢氧化物时,开始沉淀和沉淀完全时的pH如下表:
|
|
Fe3+ |
Fe2+ |
Cu2+ |
|
开始沉淀时的pH |
2.7 |
7.6 |
5.2 |
|
完全沉淀时的pH |
3.7 |
9.6 |
6.4 |
(1)加入3% H2O2之前必须进行操作Ⅱ,操作Ⅱ的名称是 ;
H2O2参加反应的离子方程式为 。
(2)加稀氨水调节pH的目的是 ,pH应调至 范围。下列物质可用来替代稀氨水的是 。
①NaOH ②Fe2O3 ③CuO ④Na2CO3
(3)经操作Ⅰ得到粗胆矾,操作Ⅲ得到精致胆矾。两步操作相同,具体包括 、 、
过滤、 、干燥等步骤。