题目内容
2.将5mL 0.4molL -1AgNO3溶液与10mL 0.3molL -1BaCl2溶液混合,反应后溶液中离子浓度最大的是( )| A. | Ag + | B. | NO ${\;}_{3}^{-}$ | C. | Cl- | D. | Ba2+ |
分析 n(AgNO3)=0.005L×0.4mol/L=0.002mol,n(BaCl2)=0.01L×0.3mol/L=0.003mol,发生2AgNO3+BaCl2=2AgCl↓+Ba(NO3)2,以此来解答.
解答 解:n(AgNO3)=0.005L×0.4mol/L=0.002mol,n(BaCl2)=0.01L×0.3mol/L=0.003mol,
由2AgNO3+BaCl2=2AgCl↓+Ba(NO3)2,银离子完全沉淀,n(NO3-)=0.002mol,n(Ba2+)=0.003mol,n(Cl-)=0.003mol×2-0.002mol=0.004mol,溶液体积相同,反应后溶液中离子浓度最大的是Cl-,
故选C.
点评 本题考查化学反应方程式的计算,为高频考点,把握发生的反应、物质的量的关系为解答的关键,侧重分析与计算能力的考查,注意银离子完全沉淀,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
12.设NA表示阿伏加德罗常数,下列叙述正确的是( )
| A. | 0.5 mol O2含氧原子数为0.5NA | B. | 1.8 g的NH4+中含有的电子数为NA | ||
| C. | 48 g O3含有的氧原子数为NA | D. | 1 mol H2O2中含NA个H2和NA个O2 |
10.下列物质中,与甲烷互为同系物的是( )
| A. | C2H4 | B. | C2H5OH | C. | C2H6 | D. | C6H6 |
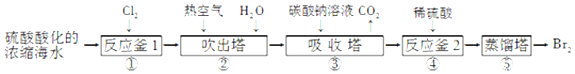
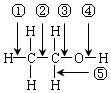 ,乙醇与钠反应时,断开的键是④;与HX反应时,断开的键是③;分子内脱水生成乙烯时,断开的键是①③;分子间脱水生成乙醚时,断开的键是③④;在铜催化作用下发生催化氧化反应时,断开的键是④⑤;酯化反应时,断开的键是④.
,乙醇与钠反应时,断开的键是④;与HX反应时,断开的键是③;分子内脱水生成乙烯时,断开的键是①③;分子间脱水生成乙醚时,断开的键是③④;在铜催化作用下发生催化氧化反应时,断开的键是④⑤;酯化反应时,断开的键是④.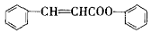 )是合成高聚酚酯的原料,其合成路线(部分反应条件略去)如图所示:
)是合成高聚酚酯的原料,其合成路线(部分反应条件略去)如图所示:
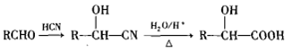
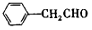 .
.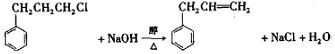 .
. .
. 或
或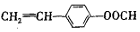 .(任写一种)
.(任写一种)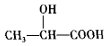 )的合成路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件).
)的合成路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件).