题目内容
有8g Na2O2、Na2O、Na2CO3、NaOH的固体混合物,与400g质量分数为3.65%的盐酸恰好反应,蒸干溶液,最终得固体质量为
A.16g B.23.4g C.31g D.无法计算
B
【解析】
试题分析:Na2O2、Na2O、Na2CO3、NaOH的混合物与盐酸反应所得溶液为氯化钠溶液,根据氯元素守恒,盐酸中的所有氯元素均进入氯化钠中,400g质量分数为3.65%的盐酸中,氯原子的物质的量是(400g×3.65%)÷36.5g/mol=0.4mol,所以氯化钠质量是0.4mol×58.5g/mol=23.4g,答案选B。
考点:考查混合物的有关计算

练习册系列答案
 学而优暑期衔接南京大学出版社系列答案
学而优暑期衔接南京大学出版社系列答案 Happy holiday欢乐假期暑假作业广东人民出版社系列答案
Happy holiday欢乐假期暑假作业广东人民出版社系列答案
相关题目

 Cl2↑+H2↑+2OH-
Cl2↑+H2↑+2OH-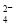 +OH-= BaSO4↓+H2O
+OH-= BaSO4↓+H2O