题目内容
 已知某可逆反应mA(g)+nB(g)?qD(g)在密闭容器中进行.
已知某可逆反应mA(g)+nB(g)?qD(g)在密闭容器中进行.(1)如图所示反应在不同时间(t),温度(T)和压强(P)与反应物B的体积分数的关系曲线.根据图象填空(前三小题填“>”、“<”或“=”):
①温度的关系:T1
②压强的关系:P1
③化学计量数的关系:m+n
④该反应的逆反应为
(2)该反应的化学平衡常数的表达式K=
(3)若该反应在一个固定容积的容器中进行,且结合
(1)中所得的计量系数的关系,可说明该反应已经达到平衡状态的是
①mv正(A)=nv逆(B)
②c(A):c(B):c(D)=m:n:q
③混合气体的平均相对分子质量保持不变
④容器内的密度保持不变
⑤容器内的压强保持不变
⑥A的物质的量保持不变.
考点:体积百分含量随温度、压强变化曲线,化学平衡状态的判断
专题:化学平衡专题
分析:(1)①②根据“先拐先平,数值大”原则,采取定一议二解答;
③根据压强越大,B的含量越高,平衡向逆反应进行来分析;
④根据温度越高,B的含量越低,平衡向正反应进行来分析;
(2)反应的化学平衡常数的表达式K=
来书写;
(3)当反应达到平衡状态时,正逆反应速率相等,各物质的浓度不再改变,由此衍生的一些物理量也不变,以此进行判断.
③根据压强越大,B的含量越高,平衡向逆反应进行来分析;
④根据温度越高,B的含量越低,平衡向正反应进行来分析;
(2)反应的化学平衡常数的表达式K=
| 各个生成物平衡浓度系数次方的乘积 |
| 各个反应物平衡浓度系数次方的乘积 |
(3)当反应达到平衡状态时,正逆反应速率相等,各物质的浓度不再改变,由此衍生的一些物理量也不变,以此进行判断.
解答:
解:(1)①定压强相同,比较温度不同时,即比较曲线T1、P2与曲线T2、P2,根据先出现拐点,先到达平衡,先出现拐点的曲线表示的温度高,所以T1>T2,故答案为:>;
②定温度相同,比较压强不同时,即比较曲线T1、P1与曲线T1、P2,根据先出现拐点,先到达平衡,先出现拐点的曲线表示的压强高,所以P1<P2,故答案为:<;
③由(2)知,压强P1<P2,由图知压强越大,B的含量越高,所以平衡向逆反应进行,增大压强,平衡向体积减小的方向移动,所以m+n<q,故答案为:<;
④由(1)知,温度T1>T2,由图知温度越高,B的含量越低,所以平衡向正反应进行,升高温度,平衡向吸热方向移动,故正反应为吸热反应,故答案为:吸热.
(2)反应的化学平衡常数的表达式K=
,故答案为:
;
(3)①化学反应速率之比等于系数之比,mv正(A)=nv逆(B)不能说明正逆反应速率相等,故错误;
②达到化学平衡时,各组分的浓度不随时间变化而变化,不一定相等,c(A):c(B):c(D)=m:n:q不能说明达到平衡,故错误;
③混合气体的平均相对分子质量M=
,质量守恒,n变化,所以当M不变,证明达到了平衡,故正确;
④容器内的密度=
,质量守恒,V不变化,密度始终不变,所以当密度不变花了,不一定平衡,故错误;
⑤反应是一个前后系数和变化的反应,当容器内的压强保持不变,证明达到了平衡,故正确;
⑥A的物质的量保持不变,体积不变,即A的浓度不随时间的变化而变化,证明达到了平衡,故正确.
故答案为:③⑤⑥.
②定温度相同,比较压强不同时,即比较曲线T1、P1与曲线T1、P2,根据先出现拐点,先到达平衡,先出现拐点的曲线表示的压强高,所以P1<P2,故答案为:<;
③由(2)知,压强P1<P2,由图知压强越大,B的含量越高,所以平衡向逆反应进行,增大压强,平衡向体积减小的方向移动,所以m+n<q,故答案为:<;
④由(1)知,温度T1>T2,由图知温度越高,B的含量越低,所以平衡向正反应进行,升高温度,平衡向吸热方向移动,故正反应为吸热反应,故答案为:吸热.
(2)反应的化学平衡常数的表达式K=
| cq(D) |
| cm(A)?cn(B) |
| cq(D) |
| cm(A)?cn(B) |
(3)①化学反应速率之比等于系数之比,mv正(A)=nv逆(B)不能说明正逆反应速率相等,故错误;
②达到化学平衡时,各组分的浓度不随时间变化而变化,不一定相等,c(A):c(B):c(D)=m:n:q不能说明达到平衡,故错误;
③混合气体的平均相对分子质量M=
| m |
| n |
④容器内的密度=
| m |
| V |
⑤反应是一个前后系数和变化的反应,当容器内的压强保持不变,证明达到了平衡,故正确;
⑥A的物质的量保持不变,体积不变,即A的浓度不随时间的变化而变化,证明达到了平衡,故正确.
故答案为:③⑤⑥.
点评:本题考查化学平衡状态的判断、影响化学反应速率和平衡移动的因素以及平衡状态的特征,注意知识的迁移和应用是关键,难度中等.

练习册系列答案
相关题目
下列措施中不能 起到节能降耗和保护环境目的是( )
| A、加大太阳能、水能、风能、地热能等能源开发力度,减少化石燃料的使用 |
| B、研制乙醇汽油技术,降低机动车辆尾气中有害气体排放 |
| C、生产、生活中,努力实现资源的循环利用 |
| D、利用高新技术,提高石油、煤、天然气产量,以满足工业生产快速发展的需求 |
以下是一些分子的比例模型,其中错误的是( )
A、 HCl |
B、 CO2 |
C、 NH3 |
D、 CH4 |

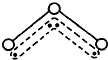 O3能吸收有害紫外线,保护人类赖以生存的空间.O3分子的结构如图,呈V型,键角116.5℃.三个原子以一个O原子为中心,与另外两个O原子分别构成一个非极性共价键;中间O原子提供2个电子,旁边两个O原子各提供1个电子,构成一个特殊的化学键--三个O原子均等地享有这4个电子.请回答:
O3能吸收有害紫外线,保护人类赖以生存的空间.O3分子的结构如图,呈V型,键角116.5℃.三个原子以一个O原子为中心,与另外两个O原子分别构成一个非极性共价键;中间O原子提供2个电子,旁边两个O原子各提供1个电子,构成一个特殊的化学键--三个O原子均等地享有这4个电子.请回答:
 某反应2A(g)?2B(g)+C(g)(吸热反应)在2L密闭容器中的三种不同条件下进行,B、C的起始浓度为0,A的浓度(mol/L)随反应时间(min)的变化情况如图所示
某反应2A(g)?2B(g)+C(g)(吸热反应)在2L密闭容器中的三种不同条件下进行,B、C的起始浓度为0,A的浓度(mol/L)随反应时间(min)的变化情况如图所示