题目内容
15.人体内所必需的下列元素中,因摄入量不足而导致贫血的是( )| A. | I | B. | Fe | C. | Ca | D. | Na |
分析 铁是合成血红蛋白的主要成分,缺铁易患贫血,以此解答该题.
解答 解:贫血与血红蛋白有关,铁是合成血红蛋白的主要成分,如铁摄入量不足,可导致贫血,其它元素与贫血无关.
故选B.
点评 本题考查化学元素与人体健康的关系,为高考考查的热点之一,题目有利于培养学生良好的科学素养,提高学习的积极性,注意相关基础知识的积累.

练习册系列答案
相关题目
5.在不同条件下分别测得反应2SO2(g)+O2(g)$?_{△}^{催化剂}$2SO3(g)的化学反应速率,其中表示该反应进行的最快的是( )
| A. | v(SO2)=4mol•L-1•min-1 | B. | v(O2)=3mol•L-1•min-1 | ||
| C. | v(SO2)=0.1mol•L-1•s-1 | D. | v(O2)=0.1mol•L-1•s-1 |
3.下列表述中合理的是( )
| A. | 在101kPa下,1g物质完全燃烧所放出的热量叫做该物质的热值 | |
| B. | 把FeCl3的水溶液加热蒸干可得到FeCl3固体 | |
| C. | 用25mL碱式滴定管量取20.00mL高锰酸钾溶液 | |
| D. | 太阳能电池是把太阳能转化为内能的装置 |
7.用酸式滴定管准确移取10.00mL某未知浓度的盐酸溶于一洁净的锥形瓶中,然后用0.20mol•L -1的氢氧化钠溶液(指示剂为酚酞).滴定结果如下:
(1)根据以上数据可以计算出盐酸的物质的量浓度为0.364mol•L-1.
(2)达到滴定终点的标志是无色变为红色,且30s内不变色.
(3)以下操作造成测定结果偏高的原因可能是AD.
A.未用标准液润洗碱式滴定管
B.滴定终点读数时,俯视滴定管的刻度,其它操作均正确
C.盛装未知液的锥形瓶用蒸馏水洗过,未用待测液润洗
D.滴定到终点读数时发现滴定管尖嘴处悬挂一滴溶液.
| NaOH起始读数 | NaOH终点读数 | |
| 第一次 | 0.50mL | 18.60mL |
| 第二次 | 0.70mL | 19.00mL |
(2)达到滴定终点的标志是无色变为红色,且30s内不变色.
(3)以下操作造成测定结果偏高的原因可能是AD.
A.未用标准液润洗碱式滴定管
B.滴定终点读数时,俯视滴定管的刻度,其它操作均正确
C.盛装未知液的锥形瓶用蒸馏水洗过,未用待测液润洗
D.滴定到终点读数时发现滴定管尖嘴处悬挂一滴溶液.
4.第四周期过渡元素常与H2O、NH3、CN-等形成配合物.
(1)Fe2+与KCN溶液反应得Fe(CN)2沉淀,当加入过量KCN溶液时沉淀溶解,形成配位数为6的配合物,写出该配合物的化学式K4[Fe(CN)6].
(2)过渡金属离子与水分子形成的配合物是否有颜色,与其d轨道电子排布有关.一般地,为do或d10排布时,无颜色;为d1一d9排布时,有颜色,如[Co(H2O)6]2+显粉红色.据此判断,[Mn(H2O)6]2+有颜色(填“无”或“有”).[Mn(H2O)6]2+配离子中存在的化学键有CD (填标号)
A.金属键 B.离子键 C.共价键 D.配位键
(3)H2S和H2O2的主要物理性质比较如表:
①H2O2分子中O原子采取sp3杂化,写出H2O2的电子式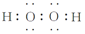
②H2S和H2O2的相对分子质量相同,造成沸点差异的主要原因是H2O2分子间形成氢键;造成溶解度差异的主要原因是H2O2分子与H2O分子间形成氢键.
(1)Fe2+与KCN溶液反应得Fe(CN)2沉淀,当加入过量KCN溶液时沉淀溶解,形成配位数为6的配合物,写出该配合物的化学式K4[Fe(CN)6].
(2)过渡金属离子与水分子形成的配合物是否有颜色,与其d轨道电子排布有关.一般地,为do或d10排布时,无颜色;为d1一d9排布时,有颜色,如[Co(H2O)6]2+显粉红色.据此判断,[Mn(H2O)6]2+有颜色(填“无”或“有”).[Mn(H2O)6]2+配离子中存在的化学键有CD (填标号)
A.金属键 B.离子键 C.共价键 D.配位键
(3)H2S和H2O2的主要物理性质比较如表:
| 沸点/K | 标准状况时在水中的溶解度 | |
| H2S | 202 | 2.6 |
| H2O2 | 423 | 以任意比互溶 |
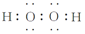
②H2S和H2O2的相对分子质量相同,造成沸点差异的主要原因是H2O2分子间形成氢键;造成溶解度差异的主要原因是H2O2分子与H2O分子间形成氢键.