题目内容
12.下列说法正确的是( )| A. | 氨水加水稀释后,溶液中c(NH3•H2O)/c(NH4+)的值减小 | |
| B. | AgCl悬浊液中加入少量KI溶液,沉淀转变为黄色,说明Ksp(AgI)>Ksp(AgCl) | |
| C. | 常温下,2NO(g)+O2(g)=2NO2(g)能够自发进行,则该反应的△H<0 | |
| D. | 相同条件下,Na2CO3溶液的碱性强于C6H5ONa,说明C6H5OH的酸性强于H2CO3 |
分析 A.氨水加水稀释后,促进一水合氨的电离;
B.加入少量KI溶液,沉淀转变为黄色,发生沉淀的转化;
C.2NO(g)+O2(g)=2NO2(g)的△S<0,△H-T△S<0的反应可自发进行;
D.Na2CO3溶液的碱性强于C6H5ONa,可知碳酸根离子水解程度大.
解答 解:A.氨水加水稀释后,促进一水合氨的电离,则溶液中n(NH3•H2O)减小,n(NH4+)增大,则溶液中c(NH3•H2O)/c(NH4+)的值减小,故A正确;
B.加入少量KI溶液,沉淀转变为黄色,发生沉淀的转化,则说明Ksp(AgI)<Ksp(AgCl),故B错误;
C.2NO(g)+O2(g)=2NO2(g)的△S<0,△H-T△S<0的反应可自发进行,则该反应能够自发进行,则该反应的△H<0,故C正确;
D.Na2CO3溶液的碱性强于C6H5ONa,可知碳酸根离子水解程度大,则酸性为苯酚大于碳酸氢根离子,故D错误;
故选AC.
点评 本题考查弱电解质的电离及沉淀转化,为高频考点,把握电离平衡移动、反应进行方向、盐类水解、沉淀转化为解本题关键,侧重分析与应用能力的考查,注意反应原理的应用,题目难度不大.

练习册系列答案
相关题目
14.下列除去杂质的操作方法不正确的是( )
| A. | 镁粉中含少量铝粉:加足量氢氧化钠溶液充分搅拌后过滤 | |
| B. | 碳酸钠溶液中含少量碳酸氢钠:加足量澄清石灰水 | |
| C. | 氯气中混有得氯化氢气体杂质:饱和食盐水 | |
| D. | 硫酸铁溶液中混有硫酸亚铁溶液:通入氯气 |
20.在无色透明的酸性溶液中,下列离子能大量共存的是( )
| A. | K+、Cu2+、NO3-、SO42- | B. | CO32-、Na-、Cl-、SO42- | ||
| C. | Al3+、Cl-、NO3-、Mg2+ | D. | H+、Ba2+、NO3-、SO42- |
7.X、Y、Z、W、M均为短周期主族元素,原子序数依次增大,X质子总数与电子层数相同,Y元素的一种同位素可用于考古时测定一些文物的年代,Z元素是空气中含量最多的元素,Y、Z、W位于同一周期,且最外层电子数之和为15,M的质子数是X、Y、Z、W四种质子数之和的$\frac{1}{2}$,下列说法正确的是( )
| A. | 原子半径M>W>Y>Z>X | |
| B. | 1molM2W2溶于足量的水中完全反应,共转移2mol电子 | |
| C. | 由X、Y、Z、W四种元素形成的化合物一定既有离子键、又有共价键 | |
| D. | 最简单气态氢化物的稳定性:W>Z>Y |
17.关于共价键,下列说法不正确的是( )
| A. | 按共用电子对是否偏移,可以把共价键划分为极性键和非极性键 | |
| B. | 按原子轨道的重叠方式,分为σ键和π 键 | |
| C. | 按共用电子对的提供方式,分为配位键和普通共价键 | |
| D. | 所有分子中都含有共价键 |
4.实验室进行NaCl溶液蒸发时,一般有以下操作过程:①放置蒸发皿;②放置酒精灯;③固定铁圈位置;④停止加热,余热蒸干;⑤加热搅拌.其正确的操作顺序为( )
| A. | ②③④⑤① | B. | ①②③④⑤ | C. | ②③①⑤④ | D. | ②①③④⑤ |
1.在盛放浓硫酸的试剂瓶上应印有如图所示警示标记中的( )
| A. |  | B. |  | C. |  | D. | 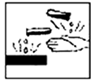 |
7.关于糖类的性质的理解正确的是( )
| A. | 糖类是由C、H、O三种元素组成,是光合作用的产物 | |
| B. | 葡糖糖是一种无色的液态,有甜味,可溶于水 | |
| C. | 淀粉和纤维素是同分异构体 | |
| D. | 纤维素在人体中酶的作用下水解成葡糖糖 |
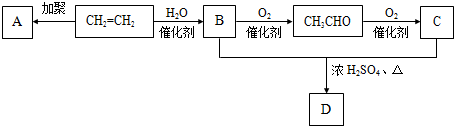
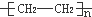 ,
,