题目内容
回答下列问题:

(1)工业合成氨的原料是氮气和氢气.氮气是从空气中分离出来的,通常使用的两种分离方法是 , ;氢气的来源是水和碳氢化合物,写出分别采用煤和天然气为原料制取氢气的化学反应方程式 , .
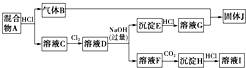
(2)设备A中含有电加热器、触煤和热交换器,设备A的名称 ,其中发生的化学反应方程式为 .
(3)设备B的名称 ,其中m和n是两个通水口,入水口是 (填“m”或“n”).不宜从相反方向通水的原因 .
(4)设备C的作用 ;
(5)在原料气制备过程中混有CO对催化剂有毒害作用,欲除去原料气中的CO,可通过如下反应来实现:CO(g)+H2O(g)?CO2 (g)+H2 (g),已知1000K时该反应的平衡常数K=0.627,若要使CO的转化超过90%,则起始物中c(H2O):c(CO)不低于 .

(1)工业合成氨的原料是氮气和氢气.氮气是从空气中分离出来的,通常使用的两种分离方法是
(2)设备A中含有电加热器、触煤和热交换器,设备A的名称
(3)设备B的名称
(4)设备C的作用
(5)在原料气制备过程中混有CO对催化剂有毒害作用,欲除去原料气中的CO,可通过如下反应来实现:CO(g)+H2O(g)?CO2 (g)+H2 (g),已知1000K时该反应的平衡常数K=0.627,若要使CO的转化超过90%,则起始物中c(H2O):c(CO)不低于
考点:工业合成氨
专题:
分析:(1)分离空气提取氮气的方法有两种,以上液化、分馏空气,另一种为空气与碳反应生成二氧化碳,反应后除去二氧化碳气体;制取氢气可用碳和水反应或甲烷与水反应;
(2)合成氨的设备为合成塔,发生N2(g)+3H2(g)
2NH3(g);
(3)冷凝分离设备为冷凝塔或冷凝器;水流和气流方向应逆向;
(4)分离器用来分离液氨和原料气;
(5)根据平衡常数用三段式法计算.
(2)合成氨的设备为合成塔,发生N2(g)+3H2(g)
| 高温高压 |
| 催化剂 |
(3)冷凝分离设备为冷凝塔或冷凝器;水流和气流方向应逆向;
(4)分离器用来分离液氨和原料气;
(5)根据平衡常数用三段式法计算.
解答:
解:(1)分离空气提取氮气的方法有两种,以上液化、分馏空气,另一种为空气与碳反应生成二氧化碳,反应后除去二氧化碳气体;C和水反应的方程式为C+H2O
CO+H2,甲烷与水反应的方程式为CH4+H2O
CO+3H2,
故答案为:液化、分馏;与碳反应后除去CO2;C+H2O
CO+H2;CH4+H2O
CO+3H2;
(2)合成氨的设备为合成塔,发生N2(g)+3H2(g)
2NH3(g),
故答案为:合成(氨)塔;N2(g)+3H2(g)
2NH3(g);
(3)冷凝分离设备为冷凝塔或冷凝器,水流和气流方向应逆向,则入水口是n,高温气体由冷凝塔上端进入,冷凝水从下端进入,可使冷水充满冷凝器,逆向冷凝效果好,
故答案为:冷凝塔或冷凝器;n;高温气体由冷凝塔上端进入,冷凝水从下端进入,逆向冷凝效果好;
(4)分离器用来分离液氨和原料气,故答案为:将液氨与未反应的原料气分离;
(5)设CO的起始浓度为xmol,H2O的起始浓度为ymol,则转化的CO的最小值为0.9x,
CO(g)+H2O(g)?CO2(g)+H2(g)
起始 x y 0 0
变化 0.9x 0.9x 0.9x 0.9x
平衡 0.1x y-0.9x 0.9x 0.9x
根据平衡常数列式:
=0.627,
解得:
=13.8.故此只要此值大于13.8,转化率就会超过90%.
故答案为:13.8.
| ||
| ||
| △ |
故答案为:液化、分馏;与碳反应后除去CO2;C+H2O
| ||
| ||
| △ |
(2)合成氨的设备为合成塔,发生N2(g)+3H2(g)
| 高温高压 |
| 催化剂 |
故答案为:合成(氨)塔;N2(g)+3H2(g)
| 高温高压 |
| 催化剂 |
(3)冷凝分离设备为冷凝塔或冷凝器,水流和气流方向应逆向,则入水口是n,高温气体由冷凝塔上端进入,冷凝水从下端进入,可使冷水充满冷凝器,逆向冷凝效果好,
故答案为:冷凝塔或冷凝器;n;高温气体由冷凝塔上端进入,冷凝水从下端进入,逆向冷凝效果好;
(4)分离器用来分离液氨和原料气,故答案为:将液氨与未反应的原料气分离;
(5)设CO的起始浓度为xmol,H2O的起始浓度为ymol,则转化的CO的最小值为0.9x,
CO(g)+H2O(g)?CO2(g)+H2(g)
起始 x y 0 0
变化 0.9x 0.9x 0.9x 0.9x
平衡 0.1x y-0.9x 0.9x 0.9x
根据平衡常数列式:
| (0.9x)2 |
| 0.1x(y-0.9x) |
解得:
| y |
| x |
故答案为:13.8.
点评:本题综合考查工业合成氨知识,涉及物质的分离、化学平衡的等问题,题目难度较大,注意把握物质的性质,根据性质选择分离方法,易错点为(5),注意利用三段式法计算较为直观.

练习册系列答案
 宝贝计划期末冲刺夺100分系列答案
宝贝计划期末冲刺夺100分系列答案 能考试全能100分系列答案
能考试全能100分系列答案
相关题目
 25℃时,在20mL0.1mol?L-1NaOH溶液中逐滴加入0.2mol?L-1醋酸溶液,pH的化曲线如图所示,有关粒子浓度关系的较中,不正确的是( )
25℃时,在20mL0.1mol?L-1NaOH溶液中逐滴加入0.2mol?L-1醋酸溶液,pH的化曲线如图所示,有关粒子浓度关系的较中,不正确的是( )| A、在A点c(Na+)>c(OH-)>c(CH3COO-)>c(H+) |
| B、在B点c(Na+)=c(CH3COO-)>c(OH-)=c(H+) |
| C、在C点c(CH3COO-)+c(CH3COOH)=2c(Na+) |
| D、在C点c(CH3COO-)>c(Na+)>c(H+)>c(OH-) |
某学生将溴乙烷和NaOH溶液共热煮沸几分钟后,冷却,滴入AgNO3溶液,结果未见到预期的现象,其主要原因是( )
| A、加热时间太短 |
| B、加AgNO3溶液前未用稀HNO3酸化 |
| C、应该和NaOH的乙醇溶液共热 |
| D、不应该冷却后再滴入AgNO3溶液 |
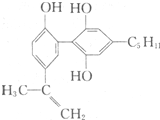 举办“人文奥运”的一个重要体现就是禁止运动员服用兴奋剂.有一种兴奋剂的结构简式如图,下列有关该物质的说法正确的是( )
举办“人文奥运”的一个重要体现就是禁止运动员服用兴奋剂.有一种兴奋剂的结构简式如图,下列有关该物质的说法正确的是( )| A、该分子中所有碳原子一定共存于同一平面中 |
| B、1 mol该物质与足量浓溴水反应时,至少消耗4 molBr2 |
| C、该物质属于苯酚同系物,则其遇FeCl3溶液一定显色 |
| D、由于该物质能使酸性KMn04溶液褪色,即可证明其分子必存在碳碳双键 |
常温下,现有1mL c1 mol/L的醋酸溶液和1mL c2mol/L的氢氧化钠溶液.下列说法中正确的是( )
| A、若c1=c2,则醋酸溶液中的c(H+)与氢氧化钠溶液中的c(OH-)相同 |
| B、若醋酸溶液的pH=3,氢氧化钠溶液的pH=11,则醋酸溶液中的c(CH3COO-)与氢氧化钠钠溶液中的c(Na+)相同 |
| C、将醋酸溶液与氢氧化钠溶液混合,若c1=c2,则所得溶液的pH=7 |
| D、将醋酸溶液与氢氧化钠溶液混合,若所得混合溶液的pH=7,则混合液中c(CH3COO-)>c(Na+) |