题目内容
18.分子式为C6H12的某烯烃,所有的碳原子都在同一平面上,则该烯烃的结构简式为(CH3)2C=C(CH3)2名称是2,3-二甲基-2-丁烯分析 根据乙烯的结构知,要使化学式为C6H12的某烯烃的所有碳原子都在同一平面上,用甲基代替乙烯中的H原子即可;
烯烃命名应选择含有碳碳双键在内的最长碳链作为主链,从靠近双键一段开始编号;
据此解答.
解答 解:根据乙烯的结构知,要使化学式为C6H12的某烯烃的所有碳原子都在同一平面上,用甲基代替乙烯中的H原子即可,则该烯烃的结构简式为(CH3)2C=C(CH3)2,
(CH3)2C=C(CH3)2,最长碳链有4个碳原子,从左端开始编号,2,3号碳原子各有1个甲基,2号碳原子上存在碳碳双键,其系统命名为:2,3-二甲基-2-丁烯;
故答案为:(CH3)2C=C(CH3)2;2,3-二甲基-2-丁烯.
点评 本题考查了有机物结构简式的书写及系统命名,熟悉常见有机物结构特点及烷烃命名规则是解题关键,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
8.某酸性溶液中,因发生氧化还原反应而不能大量共存的是( )
| A. | Ag+、NO3-、Cl-、K+ | B. | Na+、Fe2+、Cl-、NO3- | ||
| C. | K+、Ba2+、OH-、SO42- | D. | Cu2+、NH4+、Br-、Cl- |
13.下列各组物质之间的化学反应,反应产物一定为纯净物的是( )
| A. | 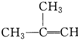 -CH3+Br2→ -CH3+Br2→ | |
| B. | CH2=CH-CH3+HCl→ | |
| C. | CH2=CH-CH=CH2+Br2→ | |
| D. | CH3-CH=CH2+H2O$→_{加热、加压}^{催化剂}$ |
3.下列有关阿佛加德罗常数(NA)的说法错误的是( )
| A. | 0.5mol H2O含有的原子数目为1.5NA | |
| B. | 32g O2所含的原子数目为NA | |
| C. | 1mol H2O含有的H2O分子数目为NA | |
| D. | 0.5NA个氯气分子的物质的量是0.5mol |
10.下列有关Cl、N、S等非金属元素化合物的说法不正确的是( )
| A. | 漂白粉的主要成分为次氯酸钙 | |
| B. | 实验室可用浓硫酸干燥氨气 | |
| C. | 实验室可用NaOH溶液处理NO2和HCl废气 | |
| D. | 从海水可获得在常温下为液体的单质是Br2 |
7.下列有关物质的性质或应用的说法正确的是( )
| A. | 在甲苯中加入少量酸性高锰酸钾溶液,振荡后褪色,正确的解释是由于侧链与苯环的相互影响,使侧链和苯环均易被氧化 | |
| B. | 用核磁共振氢谱鉴别1-丙醇、2-丙醇 | |
| C. | 间二溴苯仅有一种空间结构可证明苯分子中不存在单双键交替的结构 | |
| D. | 煤的干馏是现今获得芳香烃的主要途径 |
 .
.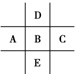 图为周期表的一部分,已知A、B、C、D、E五种元素原子核外共有85个电子,E位于周期表中第四周期,则B元素是( )
图为周期表的一部分,已知A、B、C、D、E五种元素原子核外共有85个电子,E位于周期表中第四周期,则B元素是( )