题目内容
4.下列有关化学用语表示正确的是( )| A. | 质子数和中子数均为6的碳原子:${\;}_{6}^{6}$C | |
| B. | 硫离子的结构示意图: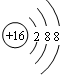 | |
| C. | 氢氧化钠的电子式: | |
| D. | 氮气分子的电子式: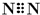 , , |
分析 A.质量数=质子数+中子数,元素符号的左上角为质量数、左下角为质子数;
B.硫离子的电荷守恒为16,核外电子总数为18,最外层含有8个电子;
C.氢氧化钠为离子化合物,电子式中需要标出阴阳离子所带电荷;
D.氮气分子中含有氮氮三键,N原子最外层满足8电子稳定结构.
解答 解:A.质子数和中子数均为6的碳原子的质量数为12,该碳原子的正确表示方法为:126C,故A错误;
B.硫离子的核电荷数为16,最外层达到8电子稳定结构,其结构示意图为: ,故B正确;
,故B正确;
C.氢氧化钠为离子化合物,钠离子和氢氧根离子应该标出所带电荷,其正确的电子式为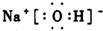 ,故C错误;
,故C错误;
D.氮原子未成键的孤对电子对未画出,氮气分子中氮原子之间形成3对共用电子对,电子式为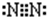 ,故D错误;
,故D错误;
故选B.
点评 本题考查了常见化学用语的表示方法,题目难度中等,涉及电子式、离子结构示意图、元素符号等知识,明确常见化学用语的书写原则为解答关键,试题培养了学生的规范答题能力.

练习册系列答案
相关题目
4.下列指定反应的离子方程式正确的是( )
| A. | NH4Al(SO4)2溶液与过量NaOH溶液反应:Al3++4OH-═AlO2-+2H2O | |
| B. | ICl溶于冷的稀KOH溶液中:ICl+2OH-═Cl-+IO-+H2O | |
| C. | 用惰性电极点解CuSO4溶液:2Cu2++4OH-$\frac{\underline{\;电解\;}}{\;}$2Cu↓+O2↑+2H2O | |
| D. | NaAlO2溶液中AlO2-的水解:AlO2-+2H2O═Al(OH)3+OH- |
15.A、B、C为短周期元素,在周期表中所处的位置如图所示,A、C两元素的原子核外电子数之和等于B原子的质子数,B原子核内质子数和中子数相等.
(1)写出A、C元素的名称氮、氟
(2)B元素最高价氧化物对应水化物的化学式为H2SO4,该化合物为共价(填“共价”或“离子”)化合物.
(3)C的原子结构示意图为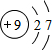 ,C的单质与H2反应的化学方程式为:H2+F2=2HF
,C的单质与H2反应的化学方程式为:H2+F2=2HF
(4)由元素A、C及氢元素形成的化合物中含有的化学键的类型有离子键、共价键.
| A | C | |
| B |
(2)B元素最高价氧化物对应水化物的化学式为H2SO4,该化合物为共价(填“共价”或“离子”)化合物.
(3)C的原子结构示意图为
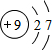 ,C的单质与H2反应的化学方程式为:H2+F2=2HF
,C的单质与H2反应的化学方程式为:H2+F2=2HF(4)由元素A、C及氢元素形成的化合物中含有的化学键的类型有离子键、共价键.
12.某有机物结构如图所示,下列说法错误的是( )
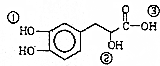

| A. | 该有机物的分子式为C9H10O5 | |
| B. | 该有机物能发生缩聚、加成、消去、氧化反应 | |
| C. | 1mol该有机物最多可以和4molNaOH发生反应 | |
| D. | 该有机物分子中①、②、③3个-OH的酸性由强到弱的顺序是③>①>② |
9.已知16S和34Se位于同一主族,下列关系正确的是( )
| A. | 原子半径:Br>Se>Cl | B. | 热稳定性:HF>HCl>H2S | ||
| C. | 还原性:S2->Se2->Cl- | D. | 酸性:HBrO4>HClO4>H2SO4 |
16.和NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 常温常压下,2.8g乙烯含有的共用电子对的数目为0.5NA | |
| B. | 标准状况下,将11.2LCl2通入足量的氢氧化钠溶液中制备漂白液,转移的电子数为NA | |
| C. | VLamol/L的氯化铁溶液中,若Fe3+的数目为NA,则Cl-的数目大于3NA | |
| D. | T℃时,1LpH=6的纯水中,含有的OH-的数目为1.0×10-8NA |
13.常温下0.1mol•L-1的CH3COOH溶液加水稀释过程中,下列表达式的数据一定变小的是( )
| A. | c(H+) | B. | c(H+)•c(OH-) | C. | $\frac{c({H}^{+})}{c(C{H}_{3}COOH)}$ | D. | $\frac{c(O{H}^{-})}{c({H}^{+})}$ |
14.下列说法正确的是( )
| A. | 石油、煤、天然气、油脂都属于化石燃料 | |
| B. | 油脂在碱性条件下的水解反应又称为皂化反应 | |
| C. | 分子式为(C6H10O5)n的淀粉和纤维素互为同分异构体 | |
| D. | 蔗糖是还原性糖,能发生银镜反应 |
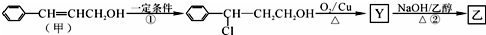
 .1mol乙最多可与5molH2反应.
.1mol乙最多可与5molH2反应.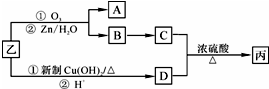
 .
. .
.