题目内容
3.下列事实中能证明碳的非金属性比硅强的是( )①往Na2SiO3溶液中通入CO2产生白色沉淀
②石墨是导体,晶体硅是半导体
③制玻璃过程中发生反应Na2CO3+SiO2$\frac{\underline{\;高温\;}}{\;}$Na2SiO3+CO2↑
④CH4比SiH4稳定.
| A. | ①④ | B. | ②③ | C. | ③④ | D. | ①② |
分析 元素的非金属性越强,其氢化物的稳定性越强,其单质的氧化性氧气,其最高价氧化物的水化物酸性越强(F、O元素除外),其单质与氢气反应越容易,据此分析解答.
解答 解:①往Na2SiO3溶液中通入CO2产生白色沉淀,碳酸和硅酸钠反应生成硅酸,说明碳酸酸性大于硅酸,说明非金属性C>Si,故正确;
②石墨是导体,晶体硅是半导体,与非金属性强弱无关,不能据此判断非金属性强弱,故错误;
③制玻璃过程中发生反应:Na2CO3+SiO2$\frac{\underline{\;高温\;}}{\;}$Na2SiO3+CO2↑,为高温固体之间的反应,不能比较非金属性,故错误;
④CH4比SiH4稳定,说明非金属性C>Si,故正确;
故选A.
点评 本题考查非金属性强弱判断,为高频考点,明确非金属性强弱判断方法是解本题关键,非金属性强弱与得电子难易程度有关,与得电子多少无关,为易错题.

练习册系列答案
 举一反三期末百分冲刺卷系列答案
举一反三期末百分冲刺卷系列答案
相关题目
14.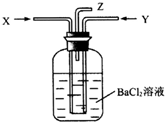 碳跟浓硫酸共热产生的混合气体X(CO2、SO2)和铜跟过量浓硝酸反应产生的气体Y(NO2)同时通入盛有足量氯化钡溶液的洗气瓶中(如图装置),下列有关说法正确的是( )
碳跟浓硫酸共热产生的混合气体X(CO2、SO2)和铜跟过量浓硝酸反应产生的气体Y(NO2)同时通入盛有足量氯化钡溶液的洗气瓶中(如图装置),下列有关说法正确的是( )
 碳跟浓硫酸共热产生的混合气体X(CO2、SO2)和铜跟过量浓硝酸反应产生的气体Y(NO2)同时通入盛有足量氯化钡溶液的洗气瓶中(如图装置),下列有关说法正确的是( )
碳跟浓硫酸共热产生的混合气体X(CO2、SO2)和铜跟过量浓硝酸反应产生的气体Y(NO2)同时通入盛有足量氯化钡溶液的洗气瓶中(如图装置),下列有关说法正确的是( )| A. | 洗气瓶中产生的沉淀是碳酸钡 | B. | 在Z导管出来的气体中无二氧化碳 | ||
| C. | 在Z导管口不会出现红棕色气体 | D. | 洗气瓶中产生的沉淀是硫酸钡 |
11.自然环境与人们的生活息息相关.下列有关说法中,不正确的是( )
| A. | 废旧显示器必须回收,其主要目的是为了提取其中的贵重金属 | |
| B. | 生活污水中所含的氮、磷化合物是植物营养素,但会导致水体污染 | |
| C. | 二氧化碳和甲烷等会导致“温室效应”,从而引起全球变暖 | |
| D. | 雾霾天气会造成严重的交通问题,雾霾是一种胶体 |
18.在反应 2X+5Y═4R+2M中,已知R 和M 的摩尔质量之比为22:9,当2.6克X与Y 完全反应,生成4.4克R,则在此反应中Y 和M 的质量比为( )
| A. | 26:9 | B. | 39:9 | C. | 40:9 | D. | 53:9 |
8.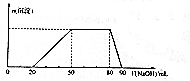 某50 mL溶液中可能含有H+、Na+、NH4+、Mg2+、Al3+、SO42-等离子,当向该溶液中加入5 mol•L-1NaOH溶液时,发现生成沉淀的物质的量n(沉淀)随NaOH溶液的体积V(NaOH)变化关系如图所示.下列说法正确的是( )
某50 mL溶液中可能含有H+、Na+、NH4+、Mg2+、Al3+、SO42-等离子,当向该溶液中加入5 mol•L-1NaOH溶液时,发现生成沉淀的物质的量n(沉淀)随NaOH溶液的体积V(NaOH)变化关系如图所示.下列说法正确的是( )
 某50 mL溶液中可能含有H+、Na+、NH4+、Mg2+、Al3+、SO42-等离子,当向该溶液中加入5 mol•L-1NaOH溶液时,发现生成沉淀的物质的量n(沉淀)随NaOH溶液的体积V(NaOH)变化关系如图所示.下列说法正确的是( )
某50 mL溶液中可能含有H+、Na+、NH4+、Mg2+、Al3+、SO42-等离子,当向该溶液中加入5 mol•L-1NaOH溶液时,发现生成沉淀的物质的量n(沉淀)随NaOH溶液的体积V(NaOH)变化关系如图所示.下列说法正确的是( )| A. | 原溶液中一定存在Mg2+、Al3+、H+、SO42- | |
| B. | 原溶液中Al3+的浓度为1mol•L-1 | |
| C. | 原溶液中NH4+的物质的量为0.4mol | |
| D. | 当加入的NaOH的溶液的体积为90mL时,反应后溶液中的离子只有Na+和SO42- |
15.类比(比较)是研究物质性质的常用方法之一,可预测许多物质的性质.但类比是相对的,不能违背客观实际.下列各说法中,正确的是( )
| A. | HCl的水溶液是强酸,HBr的水溶液也是强酸 | |
| B. | CO2气体通入Ba(NO3)2溶液中不反应,SO2气体通入Ba(NO3)2溶液中也不反应 | |
| C. | O2与Cu反应生成CuO,S与Cu反应生成CuS | |
| D. | CaCO3与稀硝酸反应生成CO2,CaSO3与稀硝酸反应生成SO2 |
17.用废旧黄铜(Cu、Zn合金,含少量Fe)制备胆矾晶体(CuSO4•5H2O)及副产物ZnO的流程为:
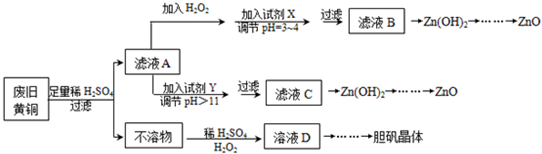
已知:①Zn及化合物性质与Al及化合物性质相似,pH>11时Zn(OH)2能溶于NaOH溶液生成[Zn(OH)4]2-.
②下表为几种离子生成氢氧化物沉淀的pH(开始沉淀时金属离子浓度为1.0mol•L-1).
(1)往滤液A中加H2O2的作用是将 Fe2+氧化为Fe3+,该反应的离子方程式为2Fe2++H2O2+2H+=2Fe3++2H2O.
(2)调节pH=3~4的试剂X可以用AC:
A.ZnO B.NaOH C.Zn(OH)2 D.ZnSO4
调节pH=3~4的目的是使Fe3+转化为Fe(OH)3,达到除去Fe3+的目的.
(3)往滤液A中加的Y试剂可以是B:
A.ZnO B.NaOH C.Na2CO3D.ZnSO4
(4)由不溶物生成溶液D的化学方程式为Cu+H2O2+H2SO4=CuSO4+2H2O.
(5)由溶液D制胆矾晶体包含的主要操作步骤是蒸发浓缩、冷却结晶、抽滤、晾干.
(6)测定胆矾晶体纯度(不含能与I-反应的杂质):准确称取0.5000g胆矾晶体置于锥形瓶,加适量水溶解,再加过量KI,用0.1000mol•L-1Na2S2O3标准溶液滴定至终点,消耗Na2S2O3标准溶液19.60mL,离子反应为:
2Cu2++4I-═2CuI(白色)↓+I2,I2+2S2O32-═2I-+S4O62-
①胆矾晶体的纯度为98.00%.
②若滴定前仰视、滴定后俯视滴定管读数,所测纯度将会偏低(填“偏高”、“偏低”或“不变”).

已知:①Zn及化合物性质与Al及化合物性质相似,pH>11时Zn(OH)2能溶于NaOH溶液生成[Zn(OH)4]2-.
②下表为几种离子生成氢氧化物沉淀的pH(开始沉淀时金属离子浓度为1.0mol•L-1).
| Fe3+ | Fe2+ | Zn2+ | |
| 开始沉淀的pH | 1.1 | 5.8 | |
| 沉淀完全的pH | 3.0 | 8.8 | 8.9 |
(2)调节pH=3~4的试剂X可以用AC:
A.ZnO B.NaOH C.Zn(OH)2 D.ZnSO4
调节pH=3~4的目的是使Fe3+转化为Fe(OH)3,达到除去Fe3+的目的.
(3)往滤液A中加的Y试剂可以是B:
A.ZnO B.NaOH C.Na2CO3D.ZnSO4
(4)由不溶物生成溶液D的化学方程式为Cu+H2O2+H2SO4=CuSO4+2H2O.
(5)由溶液D制胆矾晶体包含的主要操作步骤是蒸发浓缩、冷却结晶、抽滤、晾干.
(6)测定胆矾晶体纯度(不含能与I-反应的杂质):准确称取0.5000g胆矾晶体置于锥形瓶,加适量水溶解,再加过量KI,用0.1000mol•L-1Na2S2O3标准溶液滴定至终点,消耗Na2S2O3标准溶液19.60mL,离子反应为:
2Cu2++4I-═2CuI(白色)↓+I2,I2+2S2O32-═2I-+S4O62-
①胆矾晶体的纯度为98.00%.
②若滴定前仰视、滴定后俯视滴定管读数,所测纯度将会偏低(填“偏高”、“偏低”或“不变”).