题目内容
下列物质中所含原子数目相等的是( )
| A、2gO2和3gO3 |
| B、2gO3和3gO2 |
| C、5gCO和5gN2 |
| D、1gH2和2gO2 |
考点:物质的量的相关计算
专题:计算题
分析:根据n=
计算各物质的物质的量,结合分子中含有原子数目计算原子物质的量,据此判断.
| m |
| M |
解答:
解:A.2gO2的物质的量=
=
mol,含有原子物质的量=
mol×2=
mol,3gO3的物质的量=
=
mol,含有原子物质的量=
mol×3=
mol,二者含有原子数目不相等,故A错误;
B.2gO3的物质的量=
=
mol,含有原子物质的量=
mol×3=
mol,3gO2的物质的量=
=
mol,含有原子物质的量=
mol×2=
mol,二者含有原子数目不相等,故B错误;
C.5gCO的物质的量=
=
mol,含有原子物质的量=
mol×2=
mol,5gN2的物质的量=
=
mol,含有原子物质的量=
mol×2=
mol,含有原子数目相等,故C正确;
D.1gH2的物质的量=
=
mol,含有原子物质的量=
mol×2=1mol,2gO2的物质的量=
=
mol,含有原子物质的量=
mol×2=
mol,二者含有原子数目不相等,故D错误;
故选C.
| 2g |
| 32g/mol |
| 1 |
| 16 |
| 1 |
| 16 |
| 1 |
| 8 |
| 3g |
| 48g/mol |
| 1 |
| 16 |
| 1 |
| 16 |
| 3 |
| 16 |
B.2gO3的物质的量=
| 2g |
| 48g/mol |
| 1 |
| 24 |
| 1 |
| 24 |
| 1 |
| 8 |
| 3g |
| 32g/mol |
| 3 |
| 32 |
| 3 |
| 32 |
| 3 |
| 16 |
C.5gCO的物质的量=
| 5g |
| 28g/mol |
| 5 |
| 28 |
| 5 |
| 28 |
| 5 |
| 14 |
| 5g |
| 28g/mol |
| 5 |
| 28 |
| 5 |
| 28 |
| 5 |
| 14 |
D.1gH2的物质的量=
| 1g |
| 2g/mol |
| 1 |
| 2 |
| 1 |
| 2 |
| 2g |
| 32g/mol |
| 1 |
| 16 |
| 1 |
| 16 |
| 1 |
| 8 |
故选C.
点评:本题考查物质的量有关计算,比较基础,侧重对基础知识的巩固,注意理解化学式的意义,题目难度不大.

练习册系列答案
 新思维寒假作业系列答案
新思维寒假作业系列答案
相关题目
下列电子式中,错误的是( )
| A、Na+ |
B、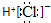 |
C、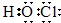 |
D、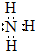 |
下列各组物质在一定条件下发生的反应不属于中和反应的是( )
| A、NH3+H2O |
| B、H2+CuO |
| C、NaHCO3+HCl |
| D、(NH4)2S+NaOH→NH3↑ |
下列关于碳氢化合物的叙述正确的是( )
| A、碳氢化合物的通式为CnH2n |
| B、石油的主要成份是碳氢化合物 |
| C、碳氢化合物都是气体 |
| D、碳氢化合物中的化学键都是极性键 |
下列反应中,调节反应物的用量或浓度,不会改变反应产物的是( )
| A、CO2和NaOH |
| B、H2SO4和锌粉 |
| C、铜和硝酸溶液 |
| D、铁粉在硫蒸气中燃烧 |
用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A、1mol Na2O2与足量的水反应,转移的电子数为2NA |
| B、7.1g Cl2完全参加反应,转移的电子数一定为0.2NA |
| C、常温常压下,0.56L甲烷中含有的共价键数为0.1NA |
| D、标准状况下,22.4L的CO2和O2组成的混合物中,含氧原子数为2NA |
对实验Ⅰ~Ⅲ的实验现象预测不正确的是( )


| A、实验Ⅰ:液体分层,下层呈无色 |
| B、实验Ⅱ:继续煮沸溶液至红褐色,停止加热,当光束通过体系时可产生丁达尔效应 |
| C、实验Ⅱ:继续煮沸至出现红褐色沉淀,停止加热,加入稀盐酸沉淀溶解 |
| D、实验Ⅲ:放置一段时间后,饱和CuSO4溶液中出现蓝色晶体 |