题目内容
指出下列反应中的氧化剂和还原剂.
(1)C+O2
CO2,氧化剂 ,还原剂 ;
(2)Zn+2H2SO4═ZnSO4+H2↑,氧化剂 ,还原剂 ;
(3)2Na+2H2O═2NaOH+H2↑,氧化剂 ,还原剂 ;
(4)Cl2+SO2+H2O═2HCl+H2SO4↑,氧化剂 ,还原剂 ;
(5)2FeCl3+2KI═2FeCl2+2KCl+I2,氧化剂 ,还原剂 .
(1)C+O2
| ||
(2)Zn+2H2SO4═ZnSO4+H2↑,氧化剂
(3)2Na+2H2O═2NaOH+H2↑,氧化剂
(4)Cl2+SO2+H2O═2HCl+H2SO4↑,氧化剂
(5)2FeCl3+2KI═2FeCl2+2KCl+I2,氧化剂
考点:氧化还原反应
专题:
分析:在氧化还原反应中,得电子化合价降低的反应物是氧化剂,失电子化合价升高的反应物是还原剂,氧化剂被氧化生成还原产物,还原剂被氧化生成氧化产物,据此分析解答.
解答:
解:在氧化还原反应中,得电子化合价降低的反应物是氧化剂,失电子化合价升高的反应物是还原剂,
(1)C+O2
CO2中C元素化合价由0价变为+4价、O元素化合价由0价变为-2价,所以O2是氧化剂、C是还原剂,故答案为:O2;C;
(2)Zn+2H2SO4═ZnSO4+H2↑中Zn元素化合价由0价变为+2价、H元素化合价由+1价变为0价,所以H2SO4是氧化剂、Zn是还原剂,故答案为:H2SO4;Zn;
(3)2Na+2H2O═2NaOH+H2↑中Na元素化合价由0价变为+1价、部分H元素化合价由+1价变为0价,所以H2O是氧化剂、Na是还原剂,故答案为:H2O;Na;
(4)Cl2+SO2+H2O═2HCl+H2SO4中Cl元素化合价由0价变为-1价、S元素化合价由+4价变为+6价,所以Cl2是氧化剂,SO2是还原剂,故答案为:Cl2;SO2;
(5)2FeCl3+2KI═2FeCl2+2KCl+I2中Fe元素化合价由+3价变为+2价、I元素化合价由-1价变为0价,所以FeCl3是氧化剂、KI是还原剂,故答案为:FeCl3;KI.
(1)C+O2
| ||
(2)Zn+2H2SO4═ZnSO4+H2↑中Zn元素化合价由0价变为+2价、H元素化合价由+1价变为0价,所以H2SO4是氧化剂、Zn是还原剂,故答案为:H2SO4;Zn;
(3)2Na+2H2O═2NaOH+H2↑中Na元素化合价由0价变为+1价、部分H元素化合价由+1价变为0价,所以H2O是氧化剂、Na是还原剂,故答案为:H2O;Na;
(4)Cl2+SO2+H2O═2HCl+H2SO4中Cl元素化合价由0价变为-1价、S元素化合价由+4价变为+6价,所以Cl2是氧化剂,SO2是还原剂,故答案为:Cl2;SO2;
(5)2FeCl3+2KI═2FeCl2+2KCl+I2中Fe元素化合价由+3价变为+2价、I元素化合价由-1价变为0价,所以FeCl3是氧化剂、KI是还原剂,故答案为:FeCl3;KI.
点评:本题考查氧化还原反应中氧化剂、还原剂判断,侧重考查基本概念,明确元素化合价变化是解本题关键,熟记常见元素化合价,题目难度不大.

练习册系列答案
 53天天练系列答案
53天天练系列答案
相关题目
设阿伏加德常数为NA.则下列说法正确的是( )
| A、常温下,2.7g铝与足量的盐酸反应,失去的电子数为0.3NA |
| B、标准状况下,0.3mol二氧化硫中含有氧原子数为0.3NA |
| C、常温常压下,18g H2O中含有的电子数为3NA |
| D、常温下,1L 0.1mol/L MgCl2溶液中含Mg2+数为0.2NA |
下列关于中和滴定实验的叙述正确的是( )
| A、锥形瓶用待测溶液润洗 |
| B、碱式滴定管可不用碱液润洗 |
| C、盐酸滴定氢氧化钠溶液时可以用甲基橙作指示剂 |
| D、滴定操作时,眼睛应注视滴定管中液面的变化 |
有X、Y、Z、W、M五种短周期元素,其中X、Y、Z、W同周期,Z、M同主族;X+与M2-具有相同的电子层结构;离子半径:Z2->W-;Y的单质晶体是一种重要的半导体材料.下列说法正确的是( )
| A、X、M两种元素形成的化合物的中一定含有离子键,不可能含有共价键 |
| B、由于W、Z、M元素的氢化物的相对分子质量依次减小,所以其沸点依次降低 |
| C、元素Y、Z、W、M的电负性高低顺序为:M>W>Z>Y |
| D、化合物ZW2的分子空间构型为直线形 |
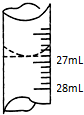 欲测定某NaOH溶液的物质的量浓度,可用0.1000mol?L-1HCl标准溶液进行中和滴定(用甲基橙作指示剂).请回答下列问题:
欲测定某NaOH溶液的物质的量浓度,可用0.1000mol?L-1HCl标准溶液进行中和滴定(用甲基橙作指示剂).请回答下列问题: