题目内容
18.将5.6克不纯的铁与足量稀硫酸反应,生成氢气0.2克.该不纯的铁含有的杂质可能是( )| A. | 碳和锌 | B. | 铁锈 | C. | 碳和铝 | D. | 碳 |
分析 根据铁与稀硫酸反应的化学方程式可以计算出5.6g纯铁能生成0.2g氢气.所以该金属可以是纯铁,也可以是含有多种杂质,但必须保证生成氢气的质量同质量时要存在比铁生成的氢气多和与酸反应生成的氢气少的物质(也可以是不与酸反应生成氢气的金属或其它杂质).
解答 解:设5.6克纯铁与稀硫酸反应生成氢气的质量为x.
Fe+H2SO4═FeSO4+H2↑
56 2
5.6g x
$\frac{56}{5.6g}=\frac{2}{x}$
x=0.2g
则该金属可以是纯铁,也可以是含有多种杂质,但必须保证生成氢气的质量同质量时要存在比铁生成的氢气多和与酸反应生成的氢气少的物质(也可以是不与酸反应生成氢气的金属或其它杂质);
由于金属与酸反应反应生成的氢气质量=金属的质量×$\frac{金属的化合价数值}{金属的相对原子质量}$,所以可得镁、铝同质量比铁生成的氢气比铁要多,而锌同质量比铁生成的氢气要少,分析选项ABD均不正确,只有C 符合题意;
故选C.
点评 本题考查了混合金属与酸反应生成氢气的质量关系,完成此类题目,可以首先采用极值法,然后采用平均值法进行.

练习册系列答案
相关题目
8.和OH-具有相同质子数和不同电子数的微粒是( )
| A. | F | B. | Cl- | C. | NH3 | D. | NH2- |
13.若元素X、Y是同主族,X元素最高价氧化物对应水化物的碱性比Y强,下列有关X、Y元素及其单质和化合物的性质判断正确的是( )
| A. | 原子半径:X>Y | |
| B. | 失电子能力:X<Y | |
| C. | 对应简单离子的氧化性:X>Y | |
| D. | X元素的单质跟酸反应置换出氢气比Y容易 |
10.下列用来表示物质变化的化学用语中,正确的是( )
| A. | 碱性氢氧燃料电池的负极反应式:O2+2H2O+4e-=4OH- | |
| B. | 粗铜精炼时,与电源正极相连的是纯铜,电极反应式为:Cu-2e-=Cu2+ | |
| C. | 用惰性电极分别电解熔融氯化钠和饱和食盐水时,阳极的电极反应式均为:2Cl--2e-=Cl2↑ | |
| D. | 钢铁发生吸氧腐蚀时的正极反应式:Fe-2e-=Fe2+ |
7.下列表示对应化学反应的离子方程式正确的是( )
| A. | 向NaAlO2溶液中通入足量的CO2:2AlO${\;}_{2}^{-}$+CO2+3H2O=2Al(OH)3↓+CO${\;}_{3}^{2-}$ | |
| B. | (NH4)2Fe(SO4)2溶液中加入少量氢氧化钡溶液:NH${\;}_{4}^{+}$+SO${\;}_{4}^{2-}$+Ba2++OH-=BaSO4↓+NH3•H2O | |
| C. | NH4Cl浓溶液中滴加浓NaOH溶液并加热:NH${\;}_{4}^{+}$+OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O | |
| D. | 磁性氧化铁溶于稀硝酸:3Fe2++4H++NO${\;}_{3}^{-}$=3Fe3++NO↑+2H2↑ |
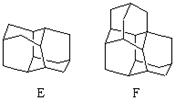 在石油中存在一种有机分子(D),X-射线衍射技术测得其结构高度对称,分子中碳原子的排列方式相当于金刚石晶胞中的部分碳原子排列,故D俗称金刚烷.图给出两种由2,3个D为基本结构单元“模块”像搭积木一样“搭”成的较复杂笼状烷的结构式.金刚烷(D)的结构式为
在石油中存在一种有机分子(D),X-射线衍射技术测得其结构高度对称,分子中碳原子的排列方式相当于金刚石晶胞中的部分碳原子排列,故D俗称金刚烷.图给出两种由2,3个D为基本结构单元“模块”像搭积木一样“搭”成的较复杂笼状烷的结构式.金刚烷(D)的结构式为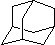 ,其中碳原子的杂化方式为sp3杂化,E的分子式为C14H20.在星际云中也发现一种高度对称的有机分子,分子式为(CH2)6N4,结构类似于金刚烷,俗称四氮金刚烷,它和金刚烷互为C(填标号).
,其中碳原子的杂化方式为sp3杂化,E的分子式为C14H20.在星际云中也发现一种高度对称的有机分子,分子式为(CH2)6N4,结构类似于金刚烷,俗称四氮金刚烷,它和金刚烷互为C(填标号).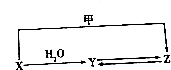 有机物X、Y、Z的转化关系如图所示(化学反应条件已省略),又己知X的储量是衡量一个国家石油化工发展水平的标志,甲是空气的主要成分之一,Y是一种常用的液体燃料.
有机物X、Y、Z的转化关系如图所示(化学反应条件已省略),又己知X的储量是衡量一个国家石油化工发展水平的标志,甲是空气的主要成分之一,Y是一种常用的液体燃料.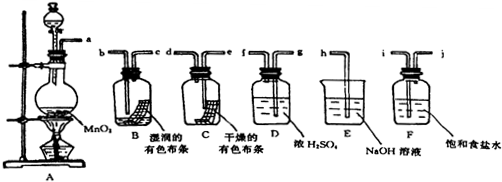
 .
.