题目内容
8.不能证明硅酸的酸性弱于碳酸酸性的实验事实是( )| A. | CO2溶于水形成碳酸,SiO2难溶于水 | |
| B. | CO2通入可溶性硅酸盐中析出硅酸沉淀 | |
| C. | 高温下SiO2与碳酸盐反应生成CO2 | |
| D. | 氯化氢通入可溶性碳酸盐溶液中放出气体,通入可溶性硅酸盐溶液中生成沉淀 |
分析 A.不能利用酸性氧化物的溶解性来比较酸性;
B.根据溶液中发生的强酸制取弱酸的原理来分析;
C.反应是在高温下固体之间的反应;
D.根据溶液中发生的强酸制取弱酸的原理及盐酸易挥发来分析.
解答 解:A.酸性强弱与水溶性没有关系,则无法据此比较酸性,故A错误;
B.CO2通入可溶性硅酸盐中析出硅酸沉淀,反应方程式是:Na2SiO3+H2O+CO2=Na2CO3+H2SiO3↓,反应原理是强酸制弱酸,说明碳酸比硅酸酸性强,故B正确;
C.比较强酸制取弱酸时在溶液中进行的反应,则在高温下固体之间的反应不能得到酸性强弱的结论,故C错误;
D.HCl通入可溶性碳酸盐溶液中放出气体,通入可溶性硅酸盐溶液中生成沉淀,根据强酸制弱酸,只能说明盐酸的酸性比碳酸强,又盐酸易挥发,可溶性硅酸盐溶液中生成沉淀,可能为盐酸与硅酸盐的反应,则无法确定碳酸与硅酸的酸性的强弱,故D错误;
故选B.
点评 本题考查酸性强弱比较,题目难度不大,根据强酸制弱酸原理分析,转移必须在溶液中发生的化学反应,如C不能得出硅酸的酸性比碳酸强,试题培养了学生的分析能力及灵活应用能力.

练习册系列答案
相关题目
19.下列有关化学用语表示正确的是( )
| A. | 核内有8个中子的碳原子:${\;}_{6}^{8}$C | B. | 18O2-的结构示意图: | ||
| C. | 羟基的电子式: | D. | 淀粉和纤维素的结构简式:CH2O |
16.下列叙述正确的是( )
| A. | 凡含离子键的物质中,一定含有金属元素 | |
| B. | 非金属元素的原子间不可能形成离子化合物 | |
| C. | 离子化合物中只含有离子键 | |
| D. | 共价化合物中只含有共价键 |
3.钚是一种具有放射性的超铀元素,几位美国科学家在1940年首次发现这一元素,它目前被应用于核武器和核反应堆.下列说法正确的是( )
| A. | ${\;}_{94}^{238}$Pu、${\;}_{94}^{239}$Pu和${\;}_{94}^{240}$Pu是钚的三种同素异形体 | |
| B. | ${\;}_{94}^{238}$Pu中有94个中子 | |
| C. | ${\;}_{94}^{239}$Pu的中子数与质子数之差为51 | |
| D. | 一个${\;}_{94}^{240}$Pu的质量为240 g |
13.下列物质的水溶液在空气中加热蒸干至质量不再减少为止,能得到较纯净的原溶质的是( )
①CuSO4
②FeSO4
③K2CO3
④Ca(HCO3)2
⑤NH4HCO3
⑥KMnO4
⑦FeCl3.
①CuSO4
②FeSO4
③K2CO3
④Ca(HCO3)2
⑤NH4HCO3
⑥KMnO4
⑦FeCl3.
| A. | 仅①③ | B. | 仅①②③ | C. | 仅①③⑥ | D. | 全部都可以 |
20.有机物的结构可用“键线式”表示.如CH3-CH═CH-CH3,可简写为 .有机物X的键线式为
.有机物X的键线式为  ,下列说法不正确的是( )
,下列说法不正确的是( )
 .有机物X的键线式为
.有机物X的键线式为  ,下列说法不正确的是( )
,下列说法不正确的是( )| A. | X的化学式为C8H8 | |
| B. | 有机物Y是X的同分异构体,且属于芳香烃,则Y的结构简式为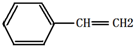 | |
| C. | X能使酸性高锰酸钾溶液褪色 | |
| D. | X与足量的H2在一定条件下反应,可生成环状的饱和烃Z,Z的一氯代物有4种 |
17.下列各组物质互为同素异形体的是( )
| A. | H、D和T | B. | 甲烷与丙烷 | C. | 乙醇与二甲醚 | D. | 红磷与白磷 |
18.下列有关实验操作、现象和结论都正确的是( )
| 操 作 | 现 象 | 结 论 | |
| A | 向煤炉中灼热的煤炭上洒少量水 | 产生淡蓝色火焰,煤炭燃烧更旺 | 加少量水后,可使煤炭燃烧放出更多的热量 |
| B | 向某溶液中滴加BaCl2溶液 | 生成白色沉淀 | 原溶液中一定有SO42- |
| C | 向某无色溶液中滴加氯水和一定量的CCl4,振荡、静置 | 下层溶液显紫红色 | 原溶液中有I- |
| D | 滴加稀NaOH溶液,并将湿润的红色石蕊试纸置于盛放溶液的试管口 | 试纸不变蓝 | 原溶液中一定无NH4+ |
| A. | A | B. | B | C. | C | D. | D |
 .
.