题目内容
氧离子的结构示意图是( )
A、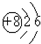 |
B、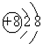 |
C、 |
D、 |
考点:原子结构示意图
专题:原子组成与结构专题
分析:氧离子含有8个质子,原子核外电子数为8+2=10,电子排布式为1S2 2S22P6,依据电子排布式判断.
解答:
解:A、氧原子含有8个质子,基态原子电子排布式为1S2 2S22P4,结构示意图为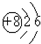 ,故A错误;
,故A错误;
B、氧离子含有8个质子,原子核外电子数为8+2=10,电子排布式为1S2 2S22P6,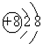 为O2-的结构示意图,故B正确;
为O2-的结构示意图,故B正确;
C、 为S的原子结构示意图,故C错误;
为S的原子结构示意图,故C错误;
D、 为Na的原子结构示意图,故D错误;
为Na的原子结构示意图,故D错误;
故选B.
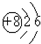 ,故A错误;
,故A错误;B、氧离子含有8个质子,原子核外电子数为8+2=10,电子排布式为1S2 2S22P6,
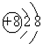 为O2-的结构示意图,故B正确;
为O2-的结构示意图,故B正确;C、
 为S的原子结构示意图,故C错误;
为S的原子结构示意图,故C错误;D、
 为Na的原子结构示意图,故D错误;
为Na的原子结构示意图,故D错误;故选B.
点评:本题考查了原子结构示意图的判断,难度不大,掌握原子的结构和原子核外电子排布规律是解题的关键.

练习册系列答案
相关题目
火法炼铜首先要焙烧黄铜矿,其反应为:2CuFeS2+O2→Cu2S+2FeS+SO2 下列说法正确的是( )
| A、Cu2S既是氧化产物又是还原产物 |
| B、每生成1 molCu2S,有4mol硫被氧化 |
| C、CuFeS2仅作还原剂,硫元素被氧化 |
| D、每转移1.2 mol电子,有0.2 mol硫被氧化 |
已知20℃,饱和KCL溶液的密度为1.174g.cm-1,物质的量浓度为4.0mol.L-1,下列说法中不正确的是( )
| A、25℃时,饱和KCL溶液的物质的量浓度大于4.0mol.L-1 |
| B、此溶液中KCL的质量分数约为25.38% |
| C、20℃时,密度小于1.174g.cm-1的KCL溶液是不饱和溶液 |
| D、将此溶液蒸发部分水,再恢复到20℃时,溶液密度一定大于1.174g.cm-1 |
关于a g H2 和b g He,下列说法正确的是( )
| A、同温、同压下,H2 和He的体积比为a:2b |
| B、同温、同压下,若a=b,则H2 和He的物质的量之比为2:1 |
| C、体积相同时,He的质量一定大于H2的质量 |
| D、同温同压下,若二者的物质的量相同,其体积也相同 |
下列说法或表示法中正确的是( )
| A、质量为53 g的碳酸钠,其物质的量为0.5 mol |
| B、等质量的氢气和氧气比较,氢气所含的分子数较少 |
| C、与1.8 g水含有相同氢原子数的硫酸的物质的量为98 g |
| D、气体摩尔体积都约为22.4 L/mol |
NA表示阿伏加德罗常数,以下说法正确的是( )
| A、常温常压下,16g氧气中含有氧原子的数目为NA |
| B、25℃,压强为1.01×105Pa时,11.2L氮气所含的原子数目为NA |
| C、标准状况下,11.2L水所含的分子数为0.5NA |
| D、标准状况下,11.2L臭氧中含NA个氧原子 |
下列溶液中的c (Cl -)与100mL 1mol?L-1氯化铝溶液中的c (Cl-)相等( )
| A、300mL1mol?L-1 氯化钠溶液 |
| B、150mL2mol?L-1氯化铵溶液 |
| C、75mL3mol?L-1 氯化钙溶液 |
| D、10mL1.5mol?L-1 氯化钡溶液 |
下列说法中正确的是( )
| A、H2的摩尔质量是2g |
| B、H2的摩尔质量是2g/mol |
| C、H2的质量是2g |
| D、1摩尔H2的质量是2g/mol |