题目内容
把5.0g镁铝合金的粉末放入到过量的NaOH溶液中,得到5.6LH2(标准状况).试计算:
(1)该合金中铝的质量分数;
(2)该合金中铝和镁的物质的量之比.
(1)该合金中铝的质量分数;
(2)该合金中铝和镁的物质的量之比.
考点:化学方程式的有关计算
专题:计算题
分析:(1)发生反应2Al+2NaOH+2H2O=2NaAlO2+3H2↑,利用生成的氢气体积根据方程式计算Al的物质的量,再计算Al的质量,进而计算Al的质量分数;
(2)结合(1)中的数据计算Mg的质量,进而计算Mg的物质的量,再计算合金中铝和镁的物质的量之比.
(2)结合(1)中的数据计算Mg的质量,进而计算Mg的物质的量,再计算合金中铝和镁的物质的量之比.
解答:
解:(1)n(H2)=
=0.25mol,则:
2Al+2NaOH+2H2O=2NaAlO2+3H2↑
2 3
n(Al) 0.25mol
所以,n(Al)=
=
mol
故m(Al)=
mol×27g/mol=4.5g,
故合金中Al的质量分数=
×100%=90%
答:合金中Al的质量分数为90%.
(2)m(Mg)=5.0g-4.5g=0.5g,
则n(Mg)=
=
mol,
故合金中Al和Mg的物质的量之比=
mol:
mol=8:1,
答:合金中Al和Mg的物质的量之比为8:1.
| 5.6L |
| 22.4L/mol |
2Al+2NaOH+2H2O=2NaAlO2+3H2↑
2 3
n(Al) 0.25mol
所以,n(Al)=
| 0.25mol×2 |
| 3 |
| 1 |
| 6 |
故m(Al)=
| 1 |
| 6 |
故合金中Al的质量分数=
| 4.5g |
| 5.0g |
答:合金中Al的质量分数为90%.
(2)m(Mg)=5.0g-4.5g=0.5g,
则n(Mg)=
| 0.5g |
| 24g/mol |
| 1 |
| 48 |
故合金中Al和Mg的物质的量之比=
| 1 |
| 6 |
| 1 |
| 48 |
答:合金中Al和Mg的物质的量之比为8:1.
点评:本题考查混合物的计算、根据方程式计算,题目难度不大,也可以利用电子转移守恒计算Al的物质的量.

练习册系列答案
 一线名师权威作业本系列答案
一线名师权威作业本系列答案
相关题目
下列无色溶液中都能大量共存的离子组是( )
| A、K+、CO32-、Ag+、SO42- |
| B、Na+、Cu2+、SO42-、Cl- |
| C、NO3-、Na+、MnO4-、K+ |
| D、Ca2+、K+、Cl-、NO3- |
向2.5mL 0.2mol/L的Na2CO3溶液中慢慢加入0.1mol/L的盐酸7.5mL,在标况下产生CO2气体的体积是( )
| A、8.4 mL |
| B、5.6 mL |
| C、4.2 mL |
| D、2.8 mL |
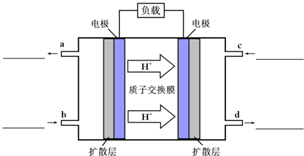 甲醇-空气燃料电池(DMFC)是一种高效能、轻污染电动汽车的车载电池,该燃料电池的电池反应式为:CH3OH(l)+
甲醇-空气燃料电池(DMFC)是一种高效能、轻污染电动汽车的车载电池,该燃料电池的电池反应式为:CH3OH(l)+