题目内容
4.下列离子方程式正确的是( )| A. | 向CuSO4溶液中投入Na:Cu2++2Na═Cu+2Na+ | |
| B. | 向FeCl3溶液中滴加KSCN溶液:Fe3++3SCN-═Fe(SCN)3↓ | |
| C. | 用氨水溶解Cu(OH)2:Cu(OH)2+4NH3•H2O═[Cu(NH3)4]2++2OH-+4H2O | |
| D. | 向BaCO3固体中加入过量的稀H2SO4:BaCO3+2H+═Ba2++CO2↑+H2O |
分析 A.钠与硫酸铜溶液反应生成氢氧化铜沉淀、氢气和硫酸钠,不会生成铜单质;
B.Fe3+与KSCN溶液反应生成红色溶液,没有沉淀生成;
C.氨水与氢氧化铜反应生成[Cu(NH3)4]2+;
D.碳酸钡与稀硫酸反应生成硫酸钡沉淀、二氧化碳气体和水,漏掉了生成硫酸钡的反应.
解答 解:A.向CuSO4溶液中投入Na,发生的反应为:2Na+2H2O=2NaOH+H2↑、2NaOH+CuSO4=Cu(OH)2↓+Na2SO4,则正确的离子方程式为:Cu2++2H2O+2Na═Cu(OH)2↓+2Na++H2↑,故A错误;
B.Fe3+与KSCN溶液反应生成红色溶液,正确的离子方程式为:Fe3++3SCN-?Fe(SCN)3,故B错误;
C.用氨水溶解Cu(OH)2的离子方程式为:Cu(OH)2+4NH3•H2O═[Cu(NH3)4]2++2OH-+4H2O,故C正确;
D.向BaCO3固体中加入过量的稀H2SO4,反应生成硫酸钡沉淀,正确的离子方程式为:BaCO3+SO42-+2H+═BaSO4↓+CO2↑+H2O,故D错误;
故选C.
点评 本题考查了离子方程式的判断,为高考的高频题,题目难度不大,注意掌握离子方程式的书写原则,明确离子方程式正误判断常用方法:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合原化学方程式等.

练习册系列答案
相关题目
14.已知阿伏加德罗常数的值为NA,则下列说法正确的是( )
| A. | 1 mol/L CuCl2溶液中含有的Cl-的个数为2NA | |
| B. | 16 g甲烷中含有的共用电子对数为NA | |
| C. | 常温常压,46 gNO2与N2O4的混合气体中含有的原子数为3NA | |
| D. | 4.6 g Na与适量氧气完全反应生成Na2O、Na2O2的混合物中含有的阴离子数大于0.1NA |
15.某化学小组欲探究铁及其化合物的氧化性和还原性,请回答下列问题:
(1)除胶头滴管外,你认为本实验必不可缺少的一种玻璃仪器是试管.
(2)实验目的:探究铁及其化合物的氧化性和还原性.
试剂:铁粉、FeCl3溶液、FeCl2溶液、氯水、锌片、铜片.
实验记录(按编号填写):
实验结论:
Fe只有还原性,Fe3+只有氧化性,Fe2+既有氧化性,又有还原性.
(3)根据以上结论判断,下列物质中既有氧化性,又有还原性的有:A E F.(多选)
A.Cl2 B.Na C.Na+ D.Cl- E.SO2 F.NO2
(4)亚铁盐在溶液中易被氧化,而实验室中需要纯净的亚铁盐溶液.那么保存亚铁盐溶液时应该如何防止亚铁盐氧化?
(1)除胶头滴管外,你认为本实验必不可缺少的一种玻璃仪器是试管.
(2)实验目的:探究铁及其化合物的氧化性和还原性.
试剂:铁粉、FeCl3溶液、FeCl2溶液、氯水、锌片、铜片.
实验记录(按编号填写):
| 序号 | 实验内容 | 实验现象 | 离子方程式 | 实验结论 |
| ① | 在FeCl2溶液中滴入适量氯水 | 溶液由浅绿色变为棕黄色 | ① | Fe2+具有还原性 |
| ② | 在FeCl2溶液中加入锌片 | / | Zn+Fe2+=Zn2++Fe | ② |
| ③ | 在FeCl3溶液中加入足量铁粉 | ③ | Fe+2Fe3+=3Fe2+ | Fe3+具有氧化性 |
| ④ | ④ | / | / | Fe3+具有氧化性 |
Fe只有还原性,Fe3+只有氧化性,Fe2+既有氧化性,又有还原性.
(3)根据以上结论判断,下列物质中既有氧化性,又有还原性的有:A E F.(多选)
A.Cl2 B.Na C.Na+ D.Cl- E.SO2 F.NO2
(4)亚铁盐在溶液中易被氧化,而实验室中需要纯净的亚铁盐溶液.那么保存亚铁盐溶液时应该如何防止亚铁盐氧化?
12.用NA表示阿伏伽德罗常数的值,下列说法不正确的是( )
| A. | 12.0g熔融的NaHSO4中含有的阳离子数为0.1NA | |
| B. | 2mol SO2和1mol O2在一定条件下充分反应后,所得混合气体的分子数大于2NA | |
| C. | 常温下,5.6g Fe片投入到足量的浓硝酸中,转移电子数为0.3NA | |
| D. | 常温常压下,14g乙烯和丙烯的混合气体中含有的原子总数为3NA |
19.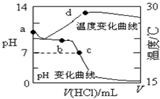 室温下,将1.000mol/L盐酸滴入20.00mL1.000mol/L氨水中,溶液pH和温度随加入盐酸体积变化曲线如图所示.下列有关说法正确的是( )
室温下,将1.000mol/L盐酸滴入20.00mL1.000mol/L氨水中,溶液pH和温度随加入盐酸体积变化曲线如图所示.下列有关说法正确的是( )
 室温下,将1.000mol/L盐酸滴入20.00mL1.000mol/L氨水中,溶液pH和温度随加入盐酸体积变化曲线如图所示.下列有关说法正确的是( )
室温下,将1.000mol/L盐酸滴入20.00mL1.000mol/L氨水中,溶液pH和温度随加入盐酸体积变化曲线如图所示.下列有关说法正确的是( )| A. | a点由水电离出的c(H+)=1.0×10-14mol/L | |
| B. | b点时c(NH4+)+c(NH3•H2O)=c(Cl-) | |
| C. | c点时消耗的盐酸体积:V(HCl)<20.00mL | |
| D. | d点后,溶液温度略下降的主要原因是NH3•H2O电离吸热 |
16.下列叙述正确的是( )
| A. | 最高价含氧酸的酸性最强的元素位于周期表的最右上方 | |
| B. | 所有主族元素的最高正化合价等于它的族序数 | |
| C. | X的含氧酸的酸性比Y的含氧酸的酸性强,则非金属性X>Y | |
| D. | 离子化合物熔融状态都能导电 |
2.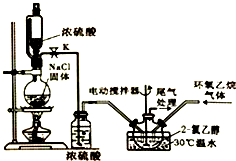 2-氯乙醇是一种重要的有机化工原料,受热时易分解.通常是以适量的2-氯乙醇为溶剂,用氯化氢与环氧乙烷反应制得新的2-氯乙醇.制取反应装置如图所示.
2-氯乙醇是一种重要的有机化工原料,受热时易分解.通常是以适量的2-氯乙醇为溶剂,用氯化氢与环氧乙烷反应制得新的2-氯乙醇.制取反应装置如图所示.
反应原理为: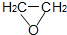 (g)+HCl(g)?ClCH2CH2OH(l)△H<0
(g)+HCl(g)?ClCH2CH2OH(l)△H<0
部分实验药品及物理量:
制取与测定实验步骤如下:
Ⅰ.2-氯乙醇的制取
①将溶剂2-氯乙醇加入三颈烧瓶中,启动搅拌器;②分别将氯化氢与环氧乙烷两种气体按6:5(物质的量)的配比通入反应器中,使其在溶剂中充分溶解反应;③反应温度控制在30℃,持续反应100min;④采用减压蒸馏,收集产品.
(1)装置中使用恒压分液漏斗的优点是平衡气压,使分液漏斗内的液体能顺利滴下.
(2)在步骤④中,采用减压分馏的原因是减小压强,使液体沸点降低,防止2-氯乙醇因温度过高而分解.
(3)写出实验步骤中提高环氧乙烷利用率的措施:氯化氢过量、反应温度控制在30℃.(写出两点)
Ⅱ.2-氯乙醇含量的测定.
已知:①ClCH2CH2OH+NaOH$\stackrel{△}{→}$HOCH2CH2OH+NaCl(水解反应)
②Ksp(AgCl)=1.8×10-30;Ksp(AgSCN)=1.0×10-12
③经检测,所得样品中还含有一定量的氯化氢和其它杂质(杂质不与NaOH和AgNO3溶液反应),密度约为1.10g•mL-1.
样品中Cl元素含量的测定,涉及的实验步骤如下:
a.待完全水解后加稀硝酸至酸性;
b.加入32.50mL0.400mol•L-1AgNO3溶液,使Cl-完全沉淀;
c.取样品1.00mL于锥形瓶中,加入NaOH溶液,加热;
d.向其中加入2.00mL硝基苯(密度:1.21g•mL-1),振荡,使沉淀表面被有机物覆盖;
e.加入指示剂,用0.100mol•L-1NH4SCN溶液滴定过量Ag+至终点,消耗NH4SCN溶液10.00mL;
f.另取样品1.00mL加水稀释成10.00mL,用pH计测定,测得溶液的pH为1.00.
(4)在上述实验步骤a-e中,
①合理的操作顺序是cabde.(选填序号)
②操作d加入硝基苯的目的是防止在滴加NH4CSN时,AgCl沉淀部分转化为AgSCN沉淀,若无此操作,则所测样品中Cl元素含量将会偏小.(填“偏大”、“偏小”或“不变”)
③操作e选用的指示剂可以是下列的C.(选填序号)
A.淀粉溶液 B.酚酞溶液 C.NH4Fe(SO4)2溶液 D.FeCl2溶液
(5)根据实验测定的数据计算,样品中2-氯乙醇的质量分数为80.50%.
(6)2-氯乙醇能否与水反应生成HCl?请设计实验验证:取少量2-氯乙醇于试管中,加水溶解,振荡后滴加硝酸银溶液,观察是否有白色沉淀,如有,则表明2-氯乙醇能与水发生反应,否则,不会反应.
 2-氯乙醇是一种重要的有机化工原料,受热时易分解.通常是以适量的2-氯乙醇为溶剂,用氯化氢与环氧乙烷反应制得新的2-氯乙醇.制取反应装置如图所示.
2-氯乙醇是一种重要的有机化工原料,受热时易分解.通常是以适量的2-氯乙醇为溶剂,用氯化氢与环氧乙烷反应制得新的2-氯乙醇.制取反应装置如图所示.反应原理为:
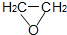 (g)+HCl(g)?ClCH2CH2OH(l)△H<0
(g)+HCl(g)?ClCH2CH2OH(l)△H<0部分实验药品及物理量:
| 化合物名称 | 相对分子质量 | 熔点(℃) | 沸点(℃) |
| 环氧乙烷 | 44 | -112,2 | 10.8 |
| 2-氯乙醇 | 80.5 | -67.5 | 128.8 |
Ⅰ.2-氯乙醇的制取
①将溶剂2-氯乙醇加入三颈烧瓶中,启动搅拌器;②分别将氯化氢与环氧乙烷两种气体按6:5(物质的量)的配比通入反应器中,使其在溶剂中充分溶解反应;③反应温度控制在30℃,持续反应100min;④采用减压蒸馏,收集产品.
(1)装置中使用恒压分液漏斗的优点是平衡气压,使分液漏斗内的液体能顺利滴下.
(2)在步骤④中,采用减压分馏的原因是减小压强,使液体沸点降低,防止2-氯乙醇因温度过高而分解.
(3)写出实验步骤中提高环氧乙烷利用率的措施:氯化氢过量、反应温度控制在30℃.(写出两点)
Ⅱ.2-氯乙醇含量的测定.
已知:①ClCH2CH2OH+NaOH$\stackrel{△}{→}$HOCH2CH2OH+NaCl(水解反应)
②Ksp(AgCl)=1.8×10-30;Ksp(AgSCN)=1.0×10-12
③经检测,所得样品中还含有一定量的氯化氢和其它杂质(杂质不与NaOH和AgNO3溶液反应),密度约为1.10g•mL-1.
样品中Cl元素含量的测定,涉及的实验步骤如下:
a.待完全水解后加稀硝酸至酸性;
b.加入32.50mL0.400mol•L-1AgNO3溶液,使Cl-完全沉淀;
c.取样品1.00mL于锥形瓶中,加入NaOH溶液,加热;
d.向其中加入2.00mL硝基苯(密度:1.21g•mL-1),振荡,使沉淀表面被有机物覆盖;
e.加入指示剂,用0.100mol•L-1NH4SCN溶液滴定过量Ag+至终点,消耗NH4SCN溶液10.00mL;
f.另取样品1.00mL加水稀释成10.00mL,用pH计测定,测得溶液的pH为1.00.
(4)在上述实验步骤a-e中,
①合理的操作顺序是cabde.(选填序号)
②操作d加入硝基苯的目的是防止在滴加NH4CSN时,AgCl沉淀部分转化为AgSCN沉淀,若无此操作,则所测样品中Cl元素含量将会偏小.(填“偏大”、“偏小”或“不变”)
③操作e选用的指示剂可以是下列的C.(选填序号)
A.淀粉溶液 B.酚酞溶液 C.NH4Fe(SO4)2溶液 D.FeCl2溶液
(5)根据实验测定的数据计算,样品中2-氯乙醇的质量分数为80.50%.
(6)2-氯乙醇能否与水反应生成HCl?请设计实验验证:取少量2-氯乙醇于试管中,加水溶解,振荡后滴加硝酸银溶液,观察是否有白色沉淀,如有,则表明2-氯乙醇能与水发生反应,否则,不会反应.

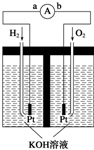 氢氧燃料电池是符合绿色化学理念的新型发电装置.如图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定.请回答:
氢氧燃料电池是符合绿色化学理念的新型发电装置.如图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定.请回答: