题目内容
9.已知反应:2X(g)+Y(g)?2Z(g).某研究小组将4mol X和2mol Y置于一容积不变的密闭容器中,测定不同时段内X的转化率,得到如下表数据:| t(min) | 2 | 4.5 | 5 | 6 |
| X转化率 | 30% | 40% | 70% | 70% |
| A. | 随着反应的进行,混合气体的密度不断增大 | |
| B. | 反应在5.5min时,v正(X)=v逆(Z) | |
| C. | 6min时,容器中剩余1.4mol Y | |
| D. | 其他条件不变,将X的物质的量改为10mol,则可得4mol Z |
分析 由表格中数据可知,5min时达到平衡,X的转化率为70%,则
2X(g)+Y(g)?2Z(g)
开始 4 2 0
转化 2.8 1.4 2.8
平衡 1.2 0.6 2.8
A.混合气体的质量不变,容积不变的密闭容器,则气体体积不变;
B.平衡时,不同物质的正逆反应速率之比等于化学计量数之比;
C.6min时物质的量不再发生变化,与5min时相同;
D.其他条件不变,将X的物质的量改为10mol,为可逆反应,2molY仍不能完全转化.
解答 解:由表格中数据可知,5min时达到平衡,X的转化率为70%,则
2X(g)+Y(g)?2Z(g)
开始 4 2 0
转化 2.8 1.4 2.8
平衡 1.2 0.6 2.8
A.混合气体的质量不变,容积不变的密闭容器,则气体体积不变,由ρ=$\frac{m}{V}$可知,密度始终不变,故A错误;
B.平衡时,不同物质的正逆反应速率之比等于化学计量数之比,则反应在5.5min时,v正(X)=v逆(Z),故B正确;
C.6min时物质的量不再发生变化,与5min时相同,则6min时,容器中剩余0.6mol Y,故C错误;
D.其他条件不变,将X的物质的量改为10mol,为可逆反应,2molY仍不能完全转化,则Z的物质的量小于4mol,故D错误;
故选B.
点评 本题考查化学平衡的计算,为高频考点,把握表格中数据应用、平衡判断、可逆反应的特征为解答的关键,侧重分析与计算能力的考查,注意选项D为易错点,题目难度不大.

 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案| A. | 用托盘天平称取3.2gNaCl固体 | |
| B. | 用10mL量筒量取7.50mL稀盐酸 | |
| C. | 固体称量时,天平游码读数0.15g | |
| D. | 用广泛pH试纸测得某溶液的pH为3.5 |
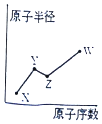 X、Y、Z、W是四种常见的短周期主族元素,其原子半径随原子序数的变化如图所示. 已知Y、Z两种元素的单质是空气的主要成分,W原子的最外层电子数与Ne原子的最外层电子数相差l.下列说法正确的是( )
X、Y、Z、W是四种常见的短周期主族元素,其原子半径随原子序数的变化如图所示. 已知Y、Z两种元素的单质是空气的主要成分,W原子的最外层电子数与Ne原子的最外层电子数相差l.下列说法正确的是( )| A. | Y、Z、W处于同一周期 | |
| B. | X、Y、Z、W的原子序数递增 | |
| C. | X、W可形成化学式为XW的离子化合物 | |
| D. | 简单离子半径是Z大于W |
| A. | 3.6mol/L | B. | 3.2mol/L | C. | 2.8mol/L | D. | 2.4mol/L |
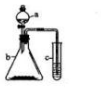 利用右下图所示的装置进行实验,将仪器a中的溶液滴入b中,根据c中所盛溶液,预测c中现象正确的是( )
利用右下图所示的装置进行实验,将仪器a中的溶液滴入b中,根据c中所盛溶液,预测c中现象正确的是( )| 选项 | a | b | c | c试管中的现象 |
| A | 浓盐酸 | KMnO4 | FeCl2溶液 | 溶液变棕黄色 |
| B | 稀硫酸 | Na2S2O3 | 溴水 | 产生浅黄色沉淀 |
| C | 饱和NaCl | CaC2 | 硫酸铜溶液 | 产生蓝色沉淀 |
| D | 浓硝酸 | 铁片 | KI-淀粉溶液 | 溶液变蓝色 |
| A. | A | B. | B | C. | C | D. | D |

| A. | A、D所含元素的原子序数大小:A一定比D小 | |
| B. | A、F所含元素的原子半径大小:A一定比F大 | |
| C. | B、E含有化学键类型相同 | |
| D. | 若常温下D为固体,则B可以与NaOH溶液反应 |
| A. | c(SO2)=0.25 mol•L-1 | B. | c(O2)=0.12 mol•L-1 | ||
| C. | c(SO2)+c(SO3)=0.15 mol•L-1 | D. | c(SO3)+c(O2)=0.3 mol•L-1 |
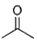 根据键线式回答下列问题:
根据键线式回答下列问题: 分子式:C5H9O2,结构简式:CH2=C(CH3)COOCH3
分子式:C5H9O2,结构简式:CH2=C(CH3)COOCH3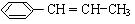 )在催化剂作用下生成聚苯丙烯的反应方程式:
)在催化剂作用下生成聚苯丙烯的反应方程式:
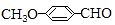 有多种的同分异构体,其中属于芳香族羧酸的同分异构体共有4种,它们的结构简式是:
有多种的同分异构体,其中属于芳香族羧酸的同分异构体共有4种,它们的结构简式是: ;
; ;
; ,
, (任意一种);、(任写其中一种)
(任意一种);、(任写其中一种) 某同学欲用下列装置探究碳与浓硫酸的反应,并对气体产物进行检验;
某同学欲用下列装置探究碳与浓硫酸的反应,并对气体产物进行检验;