题目内容
将固体NH4I置于密闭容器中,某温度下发生下列变化:
NH4I(固 )?NH3(气)+HI(气)
2HI(气)?H2(气)+I2(气)
当反应达到平衡时c(H2)=0.5mol/L,c(HI)=4mol/L,则 c(NH3)为 ;
HI 的分解率为 .
NH4I(固 )?NH3(气)+HI(气)
2HI(气)?H2(气)+I2(气)
当反应达到平衡时c(H2)=0.5mol/L,c(HI)=4mol/L,则 c(NH3)为
HI 的分解率为
考点:化学平衡的计算
专题:化学平衡专题
分析:NH4I分解出的HI为平衡与已分解的之和,即为NH4I分解出的NH3物质的量浓度,I2来自HI的分解,根据I2为0.5摩/升可知,HI分解的浓度,进而计算NH3的浓度.
解答:
解:反应达到平衡时c(H2)=0.5mol/L,根据2HI(气)?H2(气)+I2(气)可知,HI分解的浓度为2×0.5mol/L=1mol/L,反应达到平衡时c(HI)=4mol/L,所以NH4I分解平衡时生成c(HI)=4mol/L+1mol/L=5mol/L,所以平衡时NH3的浓度 c(NH3)=5mol/L,HI 的分解率为
×100%=20%,故答案:5mol/L;20%.
| 1mol/L |
| 5mol/L |
点评:本题考查化学平衡的计算,解题关键在于明白NH4I分解出的HI为平衡与已分解的之和.

练习册系列答案
 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案 暑假作业北京艺术与科学电子出版社系列答案
暑假作业北京艺术与科学电子出版社系列答案
相关题目
下列说法正确的是( )

| A、已知常温下,物质的量浓度相等的CH3COONa与CH3COOH混合液的pH<7,在此溶液中继续加CH3COONa至pH=7,测得此时c(Na+ )=c(CH3COO-)>c(CH3COOH)>c(H+)=c(OH-) |
| B、0.01 mol?L-1的Na2HPO4溶液中存在如下的平衡:HPO42-+H2O?H2PO4-+OH- HPO42-?H++PO43- 且溶液pH>7;加水稀释后溶液中HPO42-、PO43-、H+的浓度均减小 |
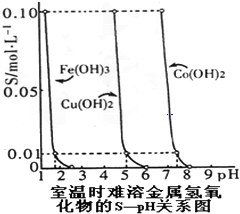
| C、图中,Y轴S表示相应金属氢氧化物在饱和溶液中阳离子的浓度,由图中数据可计算出室温下Ksp[Cu(OH)2]=1.0×10-12 |
| D、由图可知,若Fe(NO3)3溶液中含有少量的Co2+杂质,可通过加入Fe(OH)3的方法来除去 |
下列物质的性质、用途正确的是( )
| A、浓硫酸、浓硝酸都具有强氧化性,不能盛放在金属容器中 |
| B、Na2SiO3是制备硅胶和木材防火剂的原料 |
| C、明矾和漂白粉常用于自来水的净化,两者的作用原理完全相同 |
| D、合金的硬度比纯金属大,熔点也比纯金属高 |
已知298K时,Mg(OH)2的容度积常数KKsp=5.6×10-12,MgCO3容度积常数KKsp=6.8×10-6,取适量的MgCl2溶液,加入一定量的烧碱溶液达到沉淀溶解平衡,测得pH=13.0,则下列说法不正确的是( )
| A、298K时在水中溶解能力Mg(OH)2弱于MgCO3 |
| B、MgCO3悬浊液中加入适量的烧碱溶液可以生成Mg(OH)2沉淀 |
| C、沉淀溶解平衡时溶液中的c(Mg2+)=5.6×10-10mol?L-1 |
| D、298时饱和Mg(OH)2溶液与饱和MgCO3溶液相比前者的c(Mg2+)大 |
下列叙述正确的是.( )
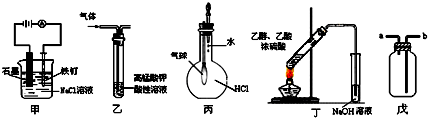
①装置甲可防止铁钉生锈
②装置乙可除去乙烯中混有的乙炔
③装置丙可验证HCl气体在水中的溶解性
④装置丁可用于实验室制取乙酸乙酯
⑤装置戊既用于收集H2、CO2、Cl2和HCl气体,也可用于干燥H2、CO2、Cl2和HCl气体.

①装置甲可防止铁钉生锈
②装置乙可除去乙烯中混有的乙炔
③装置丙可验证HCl气体在水中的溶解性
④装置丁可用于实验室制取乙酸乙酯
⑤装置戊既用于收集H2、CO2、Cl2和HCl气体,也可用于干燥H2、CO2、Cl2和HCl气体.
| A、①⑤ | B、④⑤ | C、①② | D、③⑤ |
某物质的焰色反应为浅紫色,则该物质一定是( )
| A、含有钾元素 | B、钾的化合物 |
| C、钾的单质 | D、含有钾离子 |
 (1)取一定质量H2C2O4?2H2O和KHC2O4的混合物,加水溶解,配成250mL溶液,取两份此溶液各25mL,向第一份溶液中先加入几滴酚酞试液,再滴加0.25mol?L-1 NaOH溶液至20.00mL时,溶液由无色变为浅红色;向第二份溶液中滴加适量3mol?L-1H2SO4溶液酸化后,用0.10mol?L-1KMnO4溶液滴定,消耗KMnO4溶液16.00mL时达到终点.请回答下列问题
(1)取一定质量H2C2O4?2H2O和KHC2O4的混合物,加水溶解,配成250mL溶液,取两份此溶液各25mL,向第一份溶液中先加入几滴酚酞试液,再滴加0.25mol?L-1 NaOH溶液至20.00mL时,溶液由无色变为浅红色;向第二份溶液中滴加适量3mol?L-1H2SO4溶液酸化后,用0.10mol?L-1KMnO4溶液滴定,消耗KMnO4溶液16.00mL时达到终点.请回答下列问题