题目内容
已知还原性Fe>Cu>Fe2+.现将一定量的mg铁粉加入到某x mol FeCl3和y mol CuCl2的混合溶液中,所得固体质量仍为m g,则x与y的比值可能为( )
| A、2:7 | B、3:5 |
| C、1:4 | D、4:3 |
考点:化学方程式的有关计算
专题:计算题
分析:在CuCl2和FeCl3组成的混合溶液中加入过量的铁粉,分别发生:2Fe3++Fe=3Fe2+,Fe+Cu2+=Fe2++Cu,充分反应后,所得固体质量仍为m g,则消耗的铁的质量应等于生成的铜的质量,即两个反应中固体减少质量等于固体增加质量,以此解答该题.
解答:
解:设原溶液中有x mol FeCl3,y mol CuCl2,则:
2Fe3++Fe═3Fe2+ 固体减少质量△m1
2mol 56 g
x mol 28x
Cu2++Fe═Fe2++Cu 固体增加质量△m2
1mol 8 g
y mol 8y g
因为反应前后质量相同,则28x g=8y g,即x:y=8:28=2:7,
即原溶液中FeCl3与CuCl2物质的量之比是2:7.
故选A.
2Fe3++Fe═3Fe2+ 固体减少质量△m1
2mol 56 g
x mol 28x
Cu2++Fe═Fe2++Cu 固体增加质量△m2
1mol 8 g
y mol 8y g
因为反应前后质量相同,则28x g=8y g,即x:y=8:28=2:7,
即原溶液中FeCl3与CuCl2物质的量之比是2:7.
故选A.
点评:本题考查混合物的计算,为高频考点,侧重于学生的分析能力和计算能力的考查,难度中等,注意利用差量法进行解答.

练习册系列答案
 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案
相关题目
将等质量的一小块钠分别投入等体积等浓度的HCl、H2SO4、H3PO4中,标准情况下生成氢气体积之比为( )
| A、1:1:1 |
| B、1:2:3 |
| C、3:2:1 |
| D、6:3:2 |
下列除杂方法不正确的是( )
| A、除去乙酸乙酯中混有的少量乙酸:加入饱和碳酸钠溶液,振荡、静置、分液 |
| B、除去乙醇中混有的少量水:加入适量的金属钠,充分反应后蒸馏 |
| C、除去溴苯中混有的少量溴:加入足量的氢氧化钠溶液,振荡、静置、分液 |
| D、除去96%的乙醇中的少量水制无水乙醇:加入生石灰,振荡、静置、蒸馏 |
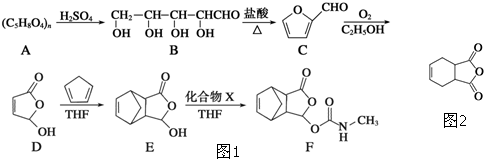
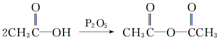 化合物G(结构如图2所示)是合成抗病毒药阿昔洛韦的中间体.请写出以OHCCH(Br)CH2CHO和1,3-丁二烯为原料制备G的合成路线流程图2(无机试剂任用).合成路线流程图示例如下:H2C=CH2
化合物G(结构如图2所示)是合成抗病毒药阿昔洛韦的中间体.请写出以OHCCH(Br)CH2CHO和1,3-丁二烯为原料制备G的合成路线流程图2(无机试剂任用).合成路线流程图示例如下:H2C=CH2