题目内容
为了测定实验室长期存放的Na2SO3固体的纯度,准确称取Wg固体样品,配成250mL溶液.设计了以下两种实验方案:
方案I:取25.00mL上述溶液,加入过量的盐酸酸化的BaCl2溶液,过滤、洗涤和干燥沉淀,称得沉淀的质量为m1g.
方案Ⅱ:取25.00mL上述溶液,加入过量的盐酸酸化的Ba(NO3)2溶液,过滤、洗涤和干燥沉淀,称重,其质量为m2g.
(1)配制250mLNa2SO3溶液时,必须用到的实验仪器有:烧杯、玻棒、胶头滴管、药匙和 、 .
(2)写出Na2SO3固体氧化变质的化学方程式 .
(3)方案I加入过量的盐酸酸化的BaCl2溶液,目的是 ,在过滤前,需要检验是否沉淀完全,其操作是 .
(4)方案I中,若滤液浑浊,将导致测定结果 (选填“偏高”或“偏低”).
(5)若操作正确,则m1 m2(选填“>”、“<”或“=”),原因是 .
(6)取25.00mL上述溶液,用滴定的方法测定Na2SO3的纯度.下列试剂可作为标准溶液进行滴定的是 .
a.酸性KMnO4溶液 b.H2O2溶液 c.Br2水 d.FeCl3溶液
Na2SO3固体的纯度可表示为: (注明你的表达式中所用的有关符号的含义和单位).
方案I:取25.00mL上述溶液,加入过量的盐酸酸化的BaCl2溶液,过滤、洗涤和干燥沉淀,称得沉淀的质量为m1g.
方案Ⅱ:取25.00mL上述溶液,加入过量的盐酸酸化的Ba(NO3)2溶液,过滤、洗涤和干燥沉淀,称重,其质量为m2g.
(1)配制250mLNa2SO3溶液时,必须用到的实验仪器有:烧杯、玻棒、胶头滴管、药匙和
(2)写出Na2SO3固体氧化变质的化学方程式
(3)方案I加入过量的盐酸酸化的BaCl2溶液,目的是
(4)方案I中,若滤液浑浊,将导致测定结果
(5)若操作正确,则m1
(6)取25.00mL上述溶液,用滴定的方法测定Na2SO3的纯度.下列试剂可作为标准溶液进行滴定的是
a.酸性KMnO4溶液 b.H2O2溶液 c.Br2水 d.FeCl3溶液
Na2SO3固体的纯度可表示为:
考点:探究物质的组成或测量物质的含量,配制一定物质的量浓度的溶液
专题:实验题
分析:(1)依据溶液配制的实验过程和操作步骤分析判断所需要的仪器,准确称取Wg固体样品,配成250mL溶液需要250ml容量瓶,由于是精确称量需要用电子天平;
(2)亚硫酸钠固体被氧气氧化为硫酸钠;
(3)方案I加入过量的盐酸酸化的BaCl2溶液是为了把亚硫酸根离子全部反应生成二氧化硫气体,使硫酸根离子全部沉淀完全;在过滤前,需要检验是否沉淀完全可以取用上层清液检验硫酸根离子是否存在设计验证;
(4)滤液浑浊说明沉淀未全部得到,称量硫酸钡沉淀质量减小,亚硫酸钠含量会增大;
(5)方案Ⅱ中加入盐酸和溶液中硝酸根离子形成稀硝酸会氧化亚硫酸钠为硫酸钠,导致硫酸钡质量增大;
(6)依据试剂的性质和滴定实验达到终点的颜色分析判断选择标准溶液;依据高锰酸钾和亚硫酸根离子反应的定量关系计算得到;
(2)亚硫酸钠固体被氧气氧化为硫酸钠;
(3)方案I加入过量的盐酸酸化的BaCl2溶液是为了把亚硫酸根离子全部反应生成二氧化硫气体,使硫酸根离子全部沉淀完全;在过滤前,需要检验是否沉淀完全可以取用上层清液检验硫酸根离子是否存在设计验证;
(4)滤液浑浊说明沉淀未全部得到,称量硫酸钡沉淀质量减小,亚硫酸钠含量会增大;
(5)方案Ⅱ中加入盐酸和溶液中硝酸根离子形成稀硝酸会氧化亚硫酸钠为硫酸钠,导致硫酸钡质量增大;
(6)依据试剂的性质和滴定实验达到终点的颜色分析判断选择标准溶液;依据高锰酸钾和亚硫酸根离子反应的定量关系计算得到;
解答:
解:(1)准确称取Wg固体样品,配成250mL溶液需要250ml容量瓶,由于是精确称量固体质量,所以需要用精确度大的电子天平;
故答案为:电子天平;250 mL的容量瓶
(2)亚硫酸钠固体被氧气氧化为硫酸钠,反应的化学方程式为:2Na2SO3+O2=2Na2SO4;
故答案为:2Na2SO3+O2=2Na2SO4;
(3)方案I加入过量的盐酸酸化的BaCl2溶液是为了把亚硫酸根离子全部反应生成二氧化硫气体,使硫酸根离子全部沉淀完全;在过滤前,需要检验是否沉淀完全可以取用上层清液检验硫酸根离子是否存在设计验证,加入氯化钡溶液,若不出现白色沉淀证明为沉淀完全,否则沉淀不完全;
故答案为:使SO32-充分转化为气体,使SO42-完全沉淀;静置,在上层清液中再滴入氯化钡溶液,观察是否继续有沉淀生成;
(4)方案I中,若滤液浑浊,滤液浑浊说明沉淀未全部得到,称量硫酸钡沉淀质量减小,亚硫酸钠含量会增大,将导致测定结果偏高;
故答案为:偏高;
(5)方案Ⅱ中加入盐酸和溶液中硝酸根离子形成稀硝酸,稀硝酸氧化亚硫酸钠为硫酸钠,加入硝酸钡导致硫酸钡质量增大;
故答案为:<,方案II中盐酸提供H+,Ba(NO3)2提供NO3-形成稀HNO3,将一部分SO32-氧化成SO42-,导致BaSO4质量增大;
(6)取25.00mL上述溶液,用滴定的方法测定Na2SO3的纯度.下列试剂可作为标准溶液进行滴定的必须是安全,反应现象明显,终点易于判断分析判断;
a.酸性KMnO4溶液 滴入最后一滴溶液由无色变化为紫红色,证明反应达到终点,故a符合;
b.H2O2溶液可以氧化亚硫酸钠为硫酸钠,大反应终点无明显现象,故b不符合;
c.Br2水 是易挥发的物物质,乙产生有毒的溴蒸气,故不做标准液,故c不符合;
d.FeCl3溶液滴入反应,溶液变化为浅绿色,溶液颜色变化不明显,不能指示反应终点,故d不符合;
故选a;
用高锰酸钾溶液滴定亚硫酸钠溶液,设高锰酸钾溶液浓度为c(KMnO4)mol/L,体积为V(KMnO4)ml,依据反应的离子方程式:2MnO4-+5SO32-+6H+=2Mn2++5SO42-+3H2O,250ml溶液中含亚硫酸钠物质的量=
×
×10-3mol,所以亚硫酸钠的纯=
×10-3×100%=
×100%;
故答案为:a,
×100%;
故答案为:电子天平;250 mL的容量瓶
(2)亚硫酸钠固体被氧气氧化为硫酸钠,反应的化学方程式为:2Na2SO3+O2=2Na2SO4;
故答案为:2Na2SO3+O2=2Na2SO4;
(3)方案I加入过量的盐酸酸化的BaCl2溶液是为了把亚硫酸根离子全部反应生成二氧化硫气体,使硫酸根离子全部沉淀完全;在过滤前,需要检验是否沉淀完全可以取用上层清液检验硫酸根离子是否存在设计验证,加入氯化钡溶液,若不出现白色沉淀证明为沉淀完全,否则沉淀不完全;
故答案为:使SO32-充分转化为气体,使SO42-完全沉淀;静置,在上层清液中再滴入氯化钡溶液,观察是否继续有沉淀生成;
(4)方案I中,若滤液浑浊,滤液浑浊说明沉淀未全部得到,称量硫酸钡沉淀质量减小,亚硫酸钠含量会增大,将导致测定结果偏高;
故答案为:偏高;
(5)方案Ⅱ中加入盐酸和溶液中硝酸根离子形成稀硝酸,稀硝酸氧化亚硫酸钠为硫酸钠,加入硝酸钡导致硫酸钡质量增大;
故答案为:<,方案II中盐酸提供H+,Ba(NO3)2提供NO3-形成稀HNO3,将一部分SO32-氧化成SO42-,导致BaSO4质量增大;
(6)取25.00mL上述溶液,用滴定的方法测定Na2SO3的纯度.下列试剂可作为标准溶液进行滴定的必须是安全,反应现象明显,终点易于判断分析判断;
a.酸性KMnO4溶液 滴入最后一滴溶液由无色变化为紫红色,证明反应达到终点,故a符合;
b.H2O2溶液可以氧化亚硫酸钠为硫酸钠,大反应终点无明显现象,故b不符合;
c.Br2水 是易挥发的物物质,乙产生有毒的溴蒸气,故不做标准液,故c不符合;
d.FeCl3溶液滴入反应,溶液变化为浅绿色,溶液颜色变化不明显,不能指示反应终点,故d不符合;
故选a;
用高锰酸钾溶液滴定亚硫酸钠溶液,设高锰酸钾溶液浓度为c(KMnO4)mol/L,体积为V(KMnO4)ml,依据反应的离子方程式:2MnO4-+5SO32-+6H+=2Mn2++5SO42-+3H2O,250ml溶液中含亚硫酸钠物质的量=
| 5×V(KMnO4)×c(KMnO4) |
| 2 |
| 250 |
| 25 |
| 25×V(KMnO4)×c(KMnO4)×126g/mol |
| W |
| 3.15V(KMnO4)×c(KMnO4) |
| W |
故答案为:a,
| 3.15V(KMnO4)×c(KMnO4) |
| W |
点评:本题考查了实验方案的分析判断,实验过程中的数据分析计算应用,滴定实验的基本操作方法和配制溶液的步骤理解应用是关键,题目难度中等.

练习册系列答案
相关题目
某溶液既能溶解Al(OH)3又能溶解H2SiO3,在该溶液中可以大量共存的离子组是( )
| A、K+ Na+ HCO3- NO3- |
| B、Na+ SO42-Cl- ClO- |
| C、H+ Mg2+ SO42- NO3- |
| D、Ag+ K+ NO3- Na+ |
下列离子方程式书写正确的是( )
| A、氯化铁溶液腐蚀铜箔:Fe3++Cu=Fe2++Cu2+ | ||||
| B、NaHCO3溶液与NaOH溶液反应:OH-+HCO3-=CO2↑+H2O | ||||
C、电解饱和食盐水:2Cl-+2H2O
| ||||
| D、SO2通入足量的氨水中:SO2+NH3+H2O═NH4++HSO3- |
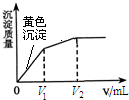 向10mL含等浓度的I-和Cl-的溶液中逐滴加入0.1mol?L-1的AgNO3溶液,沉淀的质量与加入AgNO3溶液体积的关系如图所示.下列说法不正确的是( )
向10mL含等浓度的I-和Cl-的溶液中逐滴加入0.1mol?L-1的AgNO3溶液,沉淀的质量与加入AgNO3溶液体积的关系如图所示.下列说法不正确的是( )| A、该实验可以证明AgI比AgCl更难溶 |
| B、加入V2 mL AgNO3溶液后,溶液中不含I- |
| C、V1=V2-V1 |
| D、向最终的沉淀中加入Na2S溶液,沉淀变成黑色 |
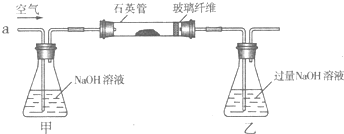
原电池与电解池在生活和生产中有着广泛应用.下列有关判断中错误的是( )

| A、装置①研究的是电解CuCl2溶液,b电极上有红色固体析出 |
| B、装置②研究的是金属的吸氧腐蚀,Fe上的反应为Fe-2e-=Fe2+ |
| C、装置③研究的是电解饱和食盐水,B电极发生的反应:2Cl--2e-=Cl2↑ |
| D、三个装置中涉及的主要反应都是氧化还原反应 |
 【化学--选修2化学与技术】
【化学--选修2化学与技术】
 已知甲、乙、丙、X、Y为中学化学常见物质,其中甲、乙、丙中均含有元素A,其转化关系如图所示(反应条件已省略):
已知甲、乙、丙、X、Y为中学化学常见物质,其中甲、乙、丙中均含有元素A,其转化关系如图所示(反应条件已省略):