题目内容
2.如图所示是实验室制备、干燥、收集气体及进行尾气处理的常见仪器装置.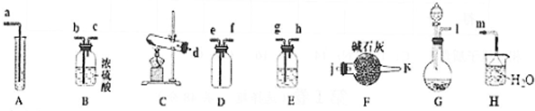
Ⅰ.实验室制取NH3、O2均可选用C或G.
(1)若用G制取O2,分液漏斗中盛装是H2O,则反应的化学方程式是2Na2O2+2H2O=4NaOH+O2↑;
(2)若用C制取NH3,则C中发生反应的化学方程式是Ca(OH)2+2NH4Cl$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2H2O+2NH3↑.
(3)选用适当的装置(可重复选用),制取、收集一瓶干燥的NH3,并吸收多余气体以防污染环境.则各装置的连接顺序是:d→j,k→f,e→j,k→m.
Ⅱ.已知强酸可以制取弱酸.
(4)请选用适当的装置(可重复选用),验证酸性:HCl>H2CO3>H2SiO3.请将所选装置的编号(如A、B、C等)和装置中的试剂按连接顺序填入下表(可以不填满,但不能增加).
| 装置编号 | |||
| 装置中的试剂 |
分析 Ⅰ.(1)若用G制取O2,分液漏斗中盛装是H2O,应为过氧化钠和水的反应制取氧气;
(2)根据固体和固体加热制取气体的原理为NH4Cl与消石灰反应生成氯化钙、氨气和水制得氨气;
(3)制取并收集干燥的NH3,则装置的连接顺序是为发生装置,干燥装置,收集装置气体沿导气管短进长出,为防止尾气吸收装置中的水蒸气进入氨气中需连接干燥装置,最后尾气处理;
Ⅱ.(4)根据较强酸制取较弱酸可知,较强酸能和较弱酸盐反应生成较弱酸,较弱酸能制取更弱的酸,要验证HCl、H2CO3、H2SiO3的酸性强弱,用盐酸和碳酸盐反应制取二氧化碳,用二氧化碳和硅酸钠溶液制取硅酸,根据实验现象确定酸的相对强弱.
解答 解:(1)若用G制取O2,分液漏斗中盛装是H2O,该装置无需加热,且水为反应物,所以选择过氧化钠和水的反应,两者反应生成氢氧化钠和氧气,化学方程式:2Na2O2+2H2O=4NaOH+O2↑,
故答案为:2Na2O2+2H2O=4NaOH+O2↑;
(2)该装置为加热固体制取氨气的装置,为NH4Cl与消石灰反应,化学反应方程式为:Ca(OH)2+2NH4Cl$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2H2O+2NH3↑,生成氯化钙、氨气和水,制得氨气,
故答案为:Ca(OH)2+2NH4Cl$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2H2O+2NH3↑;
(3)制取并收集干燥的NH3,为d,连接干燥装置,用碱石灰干燥,所以连接j、k(粗口进细口出),收集气体沿导气管短进长出连接f、e,连接干燥装置j、k,防止吸收尾气的装置中的水进入氨气中,最后尾气吸收连接m,
故答案为:j、k、f、e、m;
Ⅱ.(4)要证明HCl、H2CO3、H2SiO3的酸性强弱,G中分液漏斗盛放稀盐酸,锥形瓶中盛放碳酸钙,发生反应为CaCO3+2HCl═CO2↑+CaCl2+H2O,可证明酸性HCl>H2CO3;由于盐酸具有挥发性,制取的二氧化碳气体中含有HCl,HCl会干扰二氧化碳与硅酸钠溶液的反应,则E中盛放饱和碳酸氢钠溶液;A(或E)中盛放硅酸钠,通过二氧化碳与硅酸钠溶液反应生成硅酸的实验证明酸性:H2CO3>H2SiO3,
故答案为:
| 装置编号 | G | E | A(或E) |
| 装置中的试剂 | 稀盐酸、石灰石 | 碳酸氢钠饱和溶液 | 硅酸钠溶液 |
点评 本题考查了装置的分析应用,气体制备的试剂和反应条件分析判断,明确实验目的及装置选择是关键,题目难度中等.

 作业辅导系列答案
作业辅导系列答案 同步学典一课多练系列答案
同步学典一课多练系列答案 经典密卷系列答案
经典密卷系列答案 金牌课堂练系列答案
金牌课堂练系列答案| A. | CH4和 C3H8 | B. | CH4和C3H4 | C. | C2H2和C3H4 | D. | C2H4和C2H6 |
| A. | 溶液中大量共存:Na+、Ba2+、Cl-、CO32- | |
| B. | 无色溶液中能大量共存:NH4+、Fe3+、SO42-、CI- | |
| C. | 氢氧化铁跟硫酸反应的离子方程式是:3H++Fe(OH)3═Fe3++3H2O | |
| D. | 碳酸氢钠溶液跟氢氧化钠反应的离子方程式是:HCO3-+OH-═H2O+CO2↑ |
| A. | N2+H2→NH3 | B. | N2+O2→NO | C. | NO+O2→NO2 | D. | NO2+H2O→HNO3+NO |
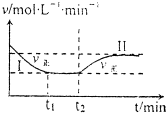 在某一恒温恒容的密闭容器中发生如下反应:3H2(g)+N2(g)?2NH3(g)△H<O.t1时刻到达平衡后,在t2时刻改变某一条件,其反应过程如图所示.下列说法正确的是( )
在某一恒温恒容的密闭容器中发生如下反应:3H2(g)+N2(g)?2NH3(g)△H<O.t1时刻到达平衡后,在t2时刻改变某一条件,其反应过程如图所示.下列说法正确的是( )| A. | Ⅰ、Ⅱ两过程达到平衡时,平衡常数:KⅠ<KⅡ | |
| B. | Ⅰ、Ⅱ两过程达到平衡时,NH3的体积分数:Ⅰ<Ⅱ | |
| C. | Ⅰ、Ⅱ两过程达到平衡的标志:气体密度不再发生变化 | |
| D. | t2时刻改变的条件可以是向密闭容器中加H2和N2混合气 |
| t/min | 0 | 2 | 4 | 7 | 9 |
| n(B)/mol | 0.32 | 0.24 | 0.22 | 0.20 | 0.20 |
| A. | 其他条件不变,向平衡体系中再充入0.32molA,再达到新平衡时,B的转化率增大 | |
| B. | 其他条件不变,降低温度,反应达到新平衡前ν(逆)>ν(正) | |
| C. | 其他条件不变,起始时向容器中充入0.64molA和B,平衡时,n(C)<0.48mol | |
| D. | 反应前2min的平均速率ν(C)=0.004mol•(L•min)-1 |
| 序号 | 检验方法 | 结论 |
| A | 向一种未知溶液中加入盐酸,产生能使澄清石灰水变浑浊的无色无味的气体 | 未知溶液中一定含有CO${\;}_{3}^{2-}$ |
| B | 向一种未知溶液中滴加NaOH溶液,产生白色沉淀 | 未知溶液中一定含有Al3+ |
| C | 向一种未知溶液中先加入盐酸酸化,再加AgNO3溶液,有白色沉淀生成 | 未知溶液中一定含有Cl- |
| D | 用洁净的铂丝蘸取一种未知液在酒精灯外焰上灼烧火焰呈黄色 | 不能确定未知溶液中一定没有含K+ |
| A. | A | B. | B | C. | C | D. | D |