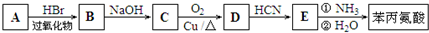题目内容
下列说法正确的是( )
| A、氯碱工业中,阴极区只需加入水 |
| B、电解熔融氯化铝制取金属铝 |
| C、电镀时,用镀层金属作阳极 |
| D、将钢闸门与外电源正极相连,可防止其腐蚀 |
考点:电解原理,金属的电化学腐蚀与防护,金属冶炼的一般原理
专题:
分析:A、电解食盐水溶液,在阴极区是氢离子失电子,在该极区域生成氢氧化钠;
B、氯化铝是共价化合物,熔融态无自由移动的离子;
C、电镀池中,镀层金属阳极,镀件是阴极,据此回答;
D、在电解池中,阳极材料易被腐蚀.
B、氯化铝是共价化合物,熔融态无自由移动的离子;
C、电镀池中,镀层金属阳极,镀件是阴极,据此回答;
D、在电解池中,阳极材料易被腐蚀.
解答:
解:A、电解食盐水溶液,在阴极区是氢离子失电子,在该极区域生成氢氧化钠,阴极区需加强电解质氢氧化钠溶液,故A错误;
B、氯化铝是共价化合物,熔融态无自由移动的离子,电解氧化铝可以得到金属铝,故B错误;
C、电镀池中,镀层金属阳极,镀件是阴极,故C正确;
D、将钢闸门与外电源正极相连,金属铁是阳极,阳极材料易被腐蚀,故D错误.
故选C.
B、氯化铝是共价化合物,熔融态无自由移动的离子,电解氧化铝可以得到金属铝,故B错误;
C、电镀池中,镀层金属阳极,镀件是阴极,故C正确;
D、将钢闸门与外电源正极相连,金属铁是阳极,阳极材料易被腐蚀,故D错误.
故选C.
点评:本题综合考查学生电解池的工作原理以及应用知识,注意知识的迁移和应用是关键,难度中等.

练习册系列答案
 一课一练课时达标系列答案
一课一练课时达标系列答案
相关题目
具有一个羟基的化合物A 10g,与乙酸反应生成乙酸某酯11.85g,并回收了未反应的A 1.3g,则A的相对分子质量为( )
| A、98 | B、116 |
| C、158 | D、278 |
泽熙同学与田中同学争论酸性与碱性食物类别,下列是碱性食物的是( )
| A、西红柿 | B、鸡蛋 |
| C、牛肉 | D、火腿肠 |
在常温下,下列有关溶液中微粒的物质的量浓度关系不正确的是( )
| A、0.1 mol?L-1 Na2S溶液中:c(OH-)=c(H+)+c(HS-)+2c(H2S) |
| B、0.1 mol?L-1 pH=8的NH4HCO3溶液中:c(HCO3-)>c(NH4+)>c(OH-)>c(H+) |
| C、浓度均为0.1 mol?L-1的NH3?H2O溶液和NH4Cl溶液等体积混合:c(NH4+)+c(H+)>c(NH3?H2O)+c(OH-) |
| D、0.1 mol?L-1 Na2S溶液与0.1 mol?L-1 NaHS溶液等体积混合:2c(Na+)-3c(S2-)=3c(HS-)+3c(H2S) |
如图所示,两个连通容器用活塞分开,左室容积为右室的两倍,但温度相同,现分别按如图所示的量充入气体,加入少量固体催化剂使左右两室内气体充分反应达到平衡,打开活塞,继续反应再次达到平衡,下列有关判断正确的是( )
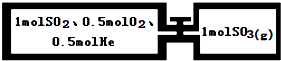

| A、通入气体未反应前,左室压强比右室大 |
| B、第一次平衡时,左室内压强一定小于右室 |
| C、第一次平衡时,SO2的物质的量右室更多 |
| D、第二次平衡时,SO2的总物质的量比第一次平衡时左室SO2的物质的量的2倍多 |

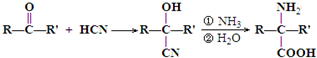
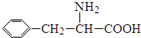 )是合成APM的原料之一.苯丙氨酸的一种合成途径如图所示:
)是合成APM的原料之一.苯丙氨酸的一种合成途径如图所示: