题目内容
18.有机物Q的分子式为C5H10O2,一定条件下Q遇NaHCO3、Na均能产生气体,且生成气体体积比(同温同压)为2:1,则Q的结构最多有( )| A. | 4种 | B. | 6种 | C. | 8种 | D. | 7种 |
分析 由有机物Q的分子式为C5H10O2,一定条件下Q遇NaHCO3、Na均能产生气体,且生成气体体积比(同温同压)为2:1,由-COOH~CO2↑、2-OH~H2↑,则分子中只有1个-COOH,结合分子式可知还含烃基为-C4H9,以此来解答.
解答 解:由有机物Q的分子式为C5H10O2,一定条件下Q遇NaHCO3、Na均能产生气体,且生成气体体积比(同温同压)为2:1,由-COOH~CO2↑、2-OH~H2↑,则分子中只有1个-COOH,结合分子式可知还含烃基为-C4H9,-C4H9有四种结构,分别为CH3-CH2-CH2-CH2-、CH3-CH2-CH(CH3)-、(CH3)2CH-CH2-、(CH3)3C-,则Q的结构最多有4种,
故选A.
点评 本题考查有机物的结构与性质,为高频考点,把握有机物的结构、有机反应、烃基的数目为解答的关键,侧重分析与应用能力的考查,注意丁基的判断,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
13.钴(Co)及其化合物在工业上有广泛应用.为从某工业废料中回收钴,某学生设计流程如图(废料中含有Al、Li、Co2O3和Fe2O3等物质).

已知:①物质溶解性:LiF难溶于水,Li2CO3微溶于水;
②部分金属离子形成氢氧化物沉淀的pH见表:
请回答:
(1)步骤Ⅰ中得到含铝溶液的反应的离子方程式是2Al+2OH-+2H2O=2AlO2-+3H2↑.
(2)写出步骤Ⅱ中Co2O3与盐酸反应的离子方程式Co2O3+6H++2Cl-=2Co2++Cl2↑+3H2O.
有同学认为Ⅱ中将盐酸换成硫酸和H2O2溶液更好,请结合离子方程式说明理由Co2O3+4H++H2O2=2Co2++3H2O+O2↑
(3)步骤Ⅲ中Na2CO3溶液的作用是调节溶液的pH,应使溶液的pH不超过7.15.废渣中的成分有LiF、Fe(OH)3.
(4)在空气中加热CoC2O4固体,经测定,210~290℃的过程中只产生CO2和一种二元化合物,该化合物中钴元素的质量分数为73.44%.此过程发生反应的化学方程式是3CoC2O4+2O2$\frac{\underline{\;210-290℃\;}}{\;}$Co3O4+6CO2.
(5)某锂离子电池的总反应为C6+LiCoO2 $?_{放电}^{充电}$ LixC6+Li1-xCoO2,LixC6中Li的化合价为0价,该锂离子电池充电时阳极的电极反应式为LiCoO2-xe-=Li1-xCoO2+xLi+.

已知:①物质溶解性:LiF难溶于水,Li2CO3微溶于水;
②部分金属离子形成氢氧化物沉淀的pH见表:
| Fe3+ | Co2+ | Co3+ | Al3+ | |
| pH(开始沉淀) | 1.9 | 7.15 | -0.23 | 3.4 |
| pH(完全沉淀) | 3.2 | 9.15 | 1.09 | 4.7 |
(1)步骤Ⅰ中得到含铝溶液的反应的离子方程式是2Al+2OH-+2H2O=2AlO2-+3H2↑.
(2)写出步骤Ⅱ中Co2O3与盐酸反应的离子方程式Co2O3+6H++2Cl-=2Co2++Cl2↑+3H2O.
有同学认为Ⅱ中将盐酸换成硫酸和H2O2溶液更好,请结合离子方程式说明理由Co2O3+4H++H2O2=2Co2++3H2O+O2↑
(3)步骤Ⅲ中Na2CO3溶液的作用是调节溶液的pH,应使溶液的pH不超过7.15.废渣中的成分有LiF、Fe(OH)3.
(4)在空气中加热CoC2O4固体,经测定,210~290℃的过程中只产生CO2和一种二元化合物,该化合物中钴元素的质量分数为73.44%.此过程发生反应的化学方程式是3CoC2O4+2O2$\frac{\underline{\;210-290℃\;}}{\;}$Co3O4+6CO2.
(5)某锂离子电池的总反应为C6+LiCoO2 $?_{放电}^{充电}$ LixC6+Li1-xCoO2,LixC6中Li的化合价为0价,该锂离子电池充电时阳极的电极反应式为LiCoO2-xe-=Li1-xCoO2+xLi+.
7.氟烷(分子式C2HF3ClBr)可以看作乙烷中的H原子被F、Br、Cl等原子取代的产物.它是一种全身麻醉药,根据你所学知识判断,它的同分异构体数目为(不考虑立体异构)( )
| A. | 3 | B. | 4 | C. | 5 | D. | 6 |
8.牙膏是由粉状摩擦剂、湿润剂、表面活性剂、粘合剂、香料、甜味剂及其它特殊成分构成的.经查文献获悉,某品牌牙膏中摩擦剂由碳酸钙、氢氧化铝组成,牙膏中其它成分不与酸、碱反应.
I.测定牙膏中摩擦剂碳酸钙的含量:利用如图所示装置进行实验,充分反应后,通过测定C中生成沉淀的质量来确定样品中碳酸钙的质量分数.图中夹持仪器略去.
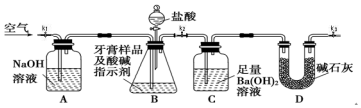
依据实验过程回答下列问题:
(1)以下检查整套装置气密性的操作正确的是a(填字母代号).
a.组装好仪器后,关闭K1和K3、打开K2,分液漏斗中装水.打开分液漏斗的两个活塞,若漏斗中水下滴一会后停止,且液面不再降低,则整套装置不漏气.
b.裝好药品后,关闭K1和K3、打开K2.打开分液漏斗的两个活塞,若漏斗中盐酸下滴一会后停止,且液面不再降低,则整套装置不漏气.
c.短时间轻微加热B,若A中溶液进入长导管,C中长导管冒气泡,则整套装置不漏气.
(2)实验过程中需持续缓慢通入空气,其作用除了可搅拌B、C中的反应物外,还有把生成的CO2气体全部排入C中,使之完全被Ba(OH)2溶液吸收.
(3)盐酸有一定程度的挥发性,为什么实验时不在B、C之间增添盛有饱和碳酸氢钠溶液的洗气装置?碳酸氢钠虽能吸收盐酸,但也产生CO2,HCl即使进入装置C中,由于Ba(OH)2是足量的,就会被Ba(OH)2中和,不会溶解BaCO3.
(4)实验中准确称取20.00g样品三份,进行三次测定,测得BaCO3平均质量为7.88g.则样品中碳酸钙的质量分数为20.0%.
II.为确定该牙膏摩擦剂中氢氧化铝的存在,请设计实验.
I.测定牙膏中摩擦剂碳酸钙的含量:利用如图所示装置进行实验,充分反应后,通过测定C中生成沉淀的质量来确定样品中碳酸钙的质量分数.图中夹持仪器略去.

依据实验过程回答下列问题:
(1)以下检查整套装置气密性的操作正确的是a(填字母代号).
a.组装好仪器后,关闭K1和K3、打开K2,分液漏斗中装水.打开分液漏斗的两个活塞,若漏斗中水下滴一会后停止,且液面不再降低,则整套装置不漏气.
b.裝好药品后,关闭K1和K3、打开K2.打开分液漏斗的两个活塞,若漏斗中盐酸下滴一会后停止,且液面不再降低,则整套装置不漏气.
c.短时间轻微加热B,若A中溶液进入长导管,C中长导管冒气泡,则整套装置不漏气.
(2)实验过程中需持续缓慢通入空气,其作用除了可搅拌B、C中的反应物外,还有把生成的CO2气体全部排入C中,使之完全被Ba(OH)2溶液吸收.
(3)盐酸有一定程度的挥发性,为什么实验时不在B、C之间增添盛有饱和碳酸氢钠溶液的洗气装置?碳酸氢钠虽能吸收盐酸,但也产生CO2,HCl即使进入装置C中,由于Ba(OH)2是足量的,就会被Ba(OH)2中和,不会溶解BaCO3.
(4)实验中准确称取20.00g样品三份,进行三次测定,测得BaCO3平均质量为7.88g.则样品中碳酸钙的质量分数为20.0%.
II.为确定该牙膏摩擦剂中氢氧化铝的存在,请设计实验.
| 实验步骤 | 预期现象与结论 |
| 取适量牙膏样品于试管中,加入足量的NaOH溶液,过滤,向滤液中滴加盐酸. | 滤液中先出现白色沉淀,随后沉淀溶解,说明该牙膏摩擦剂中含氢氧化铝. |

 .B的离子结构示意图:
.B的离子结构示意图: .D在周期表的位置:第3周期第ⅦA.写出C的原子符号2412Mg.
.D在周期表的位置:第3周期第ⅦA.写出C的原子符号2412Mg. .
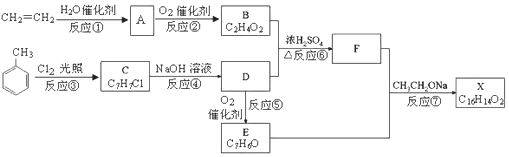
.
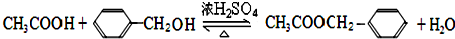 .
.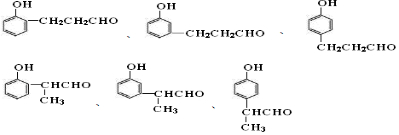 中的任意一种.
中的任意一种.