题目内容
 电解法处理含铬(六价铬)废水的原理如图所示,阳极区溶液中的离子反应是Cr2O72-+6Fe2++14H+═2Cr3++6Fe3+7H2O.下列说法正确的是( )
电解法处理含铬(六价铬)废水的原理如图所示,阳极区溶液中的离子反应是Cr2O72-+6Fe2++14H+═2Cr3++6Fe3+7H2O.下列说法正确的是( )| A、电解槽中H+向阳极移动 |
| B、阳极的电极反应式是:Fe-3e-=Fe3+ |
| C、电解一段时间后,阴极区溶液的pH升高 |
| D、阳极的铁板可用石墨代替 |
考点:电解原理
专题:
分析:由图可知,B端生成氢气,则B端氢离子得到电子,所以B为负极,则A为正极;阳极铁失去电子生成Fe2+,然后发生Cr2O72-、Fe2+的氧化还原反应.
解答:
解:A.电解槽中B端氢离子得到电子,所以B为负极,氢离子向阴极移动,故A错误;
B.阳极的电极反应式是:Fe-2e-=Fe2+,故B错误;
C.氢离子在阴极得到电子生成氢气,阴极区溶液的pH升高,故C正确;
D.阳极铁失去电子生成Fe2+,不可用石墨代替,故D错误.
故选C.
B.阳极的电极反应式是:Fe-2e-=Fe2+,故B错误;
C.氢离子在阴极得到电子生成氢气,阴极区溶液的pH升高,故C正确;
D.阳极铁失去电子生成Fe2+,不可用石墨代替,故D错误.
故选C.
点评:本题考查电解池及氧化还原反应,明确发生的电极反应是解答本题的关键,注重学生获取信息和应用信息的能力,题目难度中等.

练习册系列答案
相关题目
合金有许多特点,如:Na-K合金为液体,而单质的Na、K均为固态.据此推测钢、铁、碳三种物质中,熔点最低的是.( )
| A、钢 | B、纯铁 | C、碳 | D、无法确定 |
在3S+6KOH═2K2S+K2SO3+3H2O的反应中,被还原的硫比被氧化的硫多3.2g,则参加反应硫的物质的量为( )
| A、0.1mol |
| B、0.2mol |
| C、0.3mol |
| D、0.4mol |
将锌棒和铁棒按图示方式插入CuSO4溶液中,电流计指针发生偏转,下列针对该装置的说法正确的是( )

| A、将电能转变为化学能 |
| B、电子由铁棒流出 |
| C、锌为正极 |
| D、电池反应为:Zn+CuSO4=ZnSO4+Cu |
向0.1mol?L-1 CH3COOH溶液中加入CH3COONa晶体或加水稀释时,都会引起( )
| A、溶液的pH减小 |
| B、CH3COOH的电离程度增大 |
| C、溶液的导电能力减小 |
| D、溶液的c(OH-) 增大 |
下列事实或因果关系正确的是( )
| A、SO2的水溶液能导电说明SO2是电解质 |
| B、某溶液加NaOH溶液加热,产生气体使湿润红色石蕊试纸变蓝,则该溶液含有NH4+ |
| C、HClO是弱酸,所以NaClO是弱电解质 |
| D、某溶液中加入盐酸能产生使澄清石灰水变浑浊气体,则该溶液一定存在大量CO32- |
有关化学用语的表示正确的是( )
A、甲烷分子的比例模型是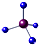 |
B、二氧化碳的电子式: |
C、Cl-的结构示意图为: |
| D、HClO的结构式为H-O-Cl |