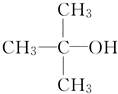
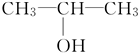
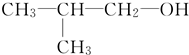题目内容
A是化合物,B是单质,它们之间相互反应以及生成物之间的转化关系如图所示: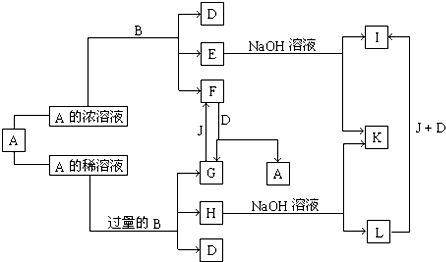
已知E溶液跟某常见有机物混合时,溶液呈紫色.请回答:
(1)B和A的浓溶液反应的条件是 ,过量B和A的稀溶液反应的化学方程式为3 .
(2)写出G和F相互转化的化学方程式:G→F .
(3)L转化成I的现象是 ; 有关的化学方程式为 .

已知E溶液跟某常见有机物混合时,溶液呈紫色.请回答:
(1)B和A的浓溶液反应的条件是
(2)写出G和F相互转化的化学方程式:G→F
(3)L转化成I的现象是
考点:无机物的推断
专题:推断题
分析:A、B是中学化学里常用的物质,其中B是单质,A是化合物;它们之间相互反应以及生成物之间的关系如图所示:已知E溶液跟NH4SCN的稀溶液混合时,溶液呈血红色,说明E含有Fe3+离子,加入氢氧化钠溶液生成氢氧化铁沉淀I为Fe(OH)3,L为Fe(OH)2,H为含Fe2+离子的溶液;K为推断B为Fe,D为H2O,J为O2,依据B和A的浓溶液反应生成的F和D反应生成G和A,判断F为NO2,A为HNO3,G为NO,所以推断出E为Fe(NO3)3,H为Fe(NO3)2,依据推断的物质回答问题.
解答:
解:A、B是中学化学里常用的物质,其中B是单质,A是化合物;它们之间相互反应以及生成物之间的关系如图所示:已知E溶液跟NH4SCN的稀溶液混合时,溶液呈血红色,说明E含有Fe3+离子,加入氢氧化钠溶液生成氢氧化铁沉淀I为Fe(OH)3,L为Fe(OH)2,H为含Fe2+离子的溶液;K为推断B为Fe,D为H2O,J为O2,依据B和A的浓溶液反应生成的F和D反应生成G和A,判断F为NO2,A为HNO3,G为NO,所以推断出E为Fe(NO3)3,H为Fe(NO3)2,
(1)Fe和浓硝酸反应条件是加热,过量Fe与稀硝酸反应生成硝酸亚铁和一氧化氮,反应方程式为3Fe+8HNO3(稀)=3Fe(NO3)2+2NO↑+4H2O,
故答案为:加热;Fe+8HNO3(稀)=3Fe(NO3)2+2NO↑+4H2O;
(2)NO与氧气反应生成NO2,反应方程式为2NO+O2=2NO2,故答案为:2NO+O2=2NO2;
(3)Fe(OH)2与氧气反应生成Fe(OH)3,白色沉淀变成灰绿色,最终变成红褐色,化学方程式为4Fe(OH)2+O2+2H2O=4Fe(OH)3,
故答案为:白色沉淀变成灰绿色,最终变成红褐色;4Fe(OH)2+O2+2H2O=4Fe(OH)3.
(1)Fe和浓硝酸反应条件是加热,过量Fe与稀硝酸反应生成硝酸亚铁和一氧化氮,反应方程式为3Fe+8HNO3(稀)=3Fe(NO3)2+2NO↑+4H2O,
故答案为:加热;Fe+8HNO3(稀)=3Fe(NO3)2+2NO↑+4H2O;
(2)NO与氧气反应生成NO2,反应方程式为2NO+O2=2NO2,故答案为:2NO+O2=2NO2;
(3)Fe(OH)2与氧气反应生成Fe(OH)3,白色沉淀变成灰绿色,最终变成红褐色,化学方程式为4Fe(OH)2+O2+2H2O=4Fe(OH)3,
故答案为:白色沉淀变成灰绿色,最终变成红褐色;4Fe(OH)2+O2+2H2O=4Fe(OH)3.
点评:本题考查了物质转化关系的推断,物质性质的应用,物质性质的分析判断,反应条件,反应现象的判断是解题关键,题目难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列说法中,正确的是( )
| A、冰融化是化学变化 |
| B、电解饱和食盐水是物理变化 |
| C、碘升华是物理变化 |
| D、原子是最小的微粒,不可再分通电 |
能使水的电离平衡右移,且水溶液显碱性的离子是( )
| A、HSO3- |
| B、OH- |
| C、Al3+ |
| D、HCO3- |
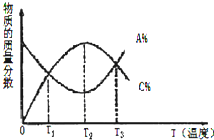 已知可逆反应:aA(g)+bB(g)?cC(g),物质的质量分数A%和C%随温度的变化曲线如图所示,下列说法正确的是( )
已知可逆反应:aA(g)+bB(g)?cC(g),物质的质量分数A%和C%随温度的变化曲线如图所示,下列说法正确的是( )| A、该反应在T1温度时达到化学平衡 |
| B、该反应在T1、T2、T3温度时,均未达到化学平衡 |
| C、升高温度,平衡向正反应方向移动 |
| D、该反应的正反应是放热反应 |
下列反应中,属于取代反应的是( )
A、CH2=CH2+HCl
| |||
B、2CH3CHO+O2
| |||
C、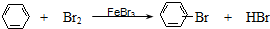 | |||
D、CH3CH2Br+NaOH
|
下列有关物质用途的叙述错误的是( )
| A、纯碱是重要的化工原料之一,可用于制化学品、清洗剂、洗涤剂 |
| B、氢氧化铝常用于治疗胃病 |
| C、NO可用于某些疾病的治疗;SO2可用于食品防腐剂 |
| D、明矾具有消毒杀菌作用,可用于净水;硫酸钡可用于钡餐透视 |
阿伏加德罗常数约为6.02×1023 mol-1,下列说法中一定正确的是( )
| A、3.4gNH3含共价键的数目约为0.2×6.02×1023个 |
| B、6.4g Cu投入300 mL 10mol/L的浓硝酸中,充分反应后转移0.2×6.02×1023个电子 |
| C、标准状况下,22.4 L SO2与11.2 L O2,混合充分反应,可得6.02×1023个SO3分子 |
| D、l L 0.5mol/L碳酸钠溶液中含有0.5×6.02×1023个CO32- |
下列有关说法正确的是( )
| A、BaSO4(s)+4C(s)═BaS(s)+4CO(g)室温下不能自发进行,说明该反应的△H>0 |
| B、纯铁和生铁在酸雨中均发生电化学腐蚀 |
| C、2SO2(g)+O2(g)?2SO3 (g);△H<0,其他条件不变时加入催化剂,SO2的反应速率和平衡转化率均增大 |
| D、自发进行的反应一定能迅速进行 |