题目内容
用NA表示阿伏伽德罗常数,下列说法中正确的是( )
| A、将1.0molFeCl3全部制成胶体,其中氢氧化铁胶粒为NA个 |
| B、1mol氧元素组成的单质一定含有2NA氧原子 |
| C、在H2O2+Cl2=2HCl+O2反应中,毎生成32g氧气,则转移2NA个电子 |
| D、含NA个Na+的 Na2O溶解于1L水中,Na+的物质的量浓度为1mol?L-1 |
考点:阿伏加德罗常数
专题:
分析:A.氯化铁是强酸弱碱盐,铁离子只有部分水解;
B.氧单质不知是氧气还是臭氧单质;
C.根据化合价的变化判断转移电子;
D.溶液的体积不等于水的体积.
B.氧单质不知是氧气还是臭氧单质;
C.根据化合价的变化判断转移电子;
D.溶液的体积不等于水的体积.
解答:
解:A.氯化铁是强酸弱碱盐,部分能发生水解生成氢氧化铁胶体,水解程度未知,所以无法计算胶粒个数,故A错误;
B.氧单质指代不明,可能是O2或O3,故B错误;
C.氧元素由-1价升高到-2价,氯元素由0价降低到-1价,该反应中电子数转移为2,故C正确;
D.溶液的体积不等于水的体积,所以含NA个Na+的Na2O溶解于1L水中形成溶液的体积不知道,无法计算其浓度,故D错误.
故选C.
B.氧单质指代不明,可能是O2或O3,故B错误;
C.氧元素由-1价升高到-2价,氯元素由0价降低到-1价,该反应中电子数转移为2,故C正确;
D.溶液的体积不等于水的体积,所以含NA个Na+的Na2O溶解于1L水中形成溶液的体积不知道,无法计算其浓度,故D错误.
故选C.
点评:本题考查阿伏加德罗常数的相关计算,题目难度不大,注意物质的组成、结构以及反应中转移的电子数等问题.

练习册系列答案
 探究与巩固河南科学技术出版社系列答案
探究与巩固河南科学技术出版社系列答案
相关题目
为了保护地下钢管不受腐蚀,可使它与( )
| A、直流电源负极相连 |
| B、铜板相连 |
| C、锡板相连 |
| D、直流电源正极相连 |
下列离子方程式书写正确的是( )
| A、浓NaOH溶液与浓CaCl2溶液混合:Ca2++2OH-=Ca(OH)2↓ |
| B、氯化铝溶液中滴加氨水生成沉淀:Al3++3OH-=Al(OH)3↓ |
| C、利用醋酸溶解含碳酸钙的水垢CaCO3+2H+=Ca2++H2O+CO2↑ |
| D、NaHSO4溶液中滴加NaHCO3溶液:2H++CO32-=CO2↑+H2O |
下列有关化学用语表示正确的是( )
| A、乙烯的结构简式:CH2CH2 |
B、羟基的电子式: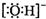 |
C、甲烷分子的比例模型: |
D、乙醇的结构式: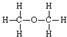 |
在一定温度下,向饱和的烧碱溶液中放入一定量的过氧化钠,充分反应后恢复到原温度,下列说法正确的是( )
| A、溶液中的Na+浓度增大,有O2放出 |
| B、溶液中的OH- 浓度不变,有H2放出 |
| C、溶液中的Na+数目减少,有O2放出 |
| D、溶液中的OH-浓度增大,有O2放出 |
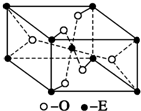 已知A、B、C、D、E五种元素的原子序数依次递增,A、B、C、D位于前三周期.A位于周期表的s区,其原子中电子层数和未成对电子数相同;B的基态原子中电子占据三种能量不同的原子轨道,且每种轨道中的电子总数相同;D原子的核外成对电子对数与未成对电子数之比为3:2.A、B、D三种元素组成的一种化合物M是新装修居室中常含有的一种有害气体,A、B两种元素组成的原子个数之比为1:1的化合物N是常见的有机溶剂.E有“生物金属”之称,E4+和氩原子的核外电子排布相同.
已知A、B、C、D、E五种元素的原子序数依次递增,A、B、C、D位于前三周期.A位于周期表的s区,其原子中电子层数和未成对电子数相同;B的基态原子中电子占据三种能量不同的原子轨道,且每种轨道中的电子总数相同;D原子的核外成对电子对数与未成对电子数之比为3:2.A、B、D三种元素组成的一种化合物M是新装修居室中常含有的一种有害气体,A、B两种元素组成的原子个数之比为1:1的化合物N是常见的有机溶剂.E有“生物金属”之称,E4+和氩原子的核外电子排布相同.