题目内容
8.今有十种物质:①铝线 ②石墨 ③CO2 ④BaSO4晶体 ⑤纯硫酸 ⑥金刚石⑦石灰水 ⑧乙醇 ⑨熔化的KNO3⑩HCl(填序号)其中,能导电的有①②⑦⑨,属于电解质的有④⑤⑨⑩,属于非电解质的有③⑧.
分析 在水溶液里或融融状态下能导电的化合物是电解质,在水溶液里或熔融状态下都不能导电的化合物是非电解质,无论是电解质还是非电解质都必须是化合物,据此分析.
解答 解:①铝线是金属单质,能导电,既不是电解质也不是非电解质;
②石墨是非金属单质,能导电,既不是电解质也不是非电解质;
③CO2 不能导电,是氧化物,属于非电解质;
④BaSO4晶体不能导电,是盐,熔融状态下完全电离,属于电解质;
⑤纯硫酸不能导电,溶于水中能导电,是电解质;
⑥金刚石不能导电,是非金属单质,既不是电解质也不是非电解质;
⑦石灰水能导电,属于混合物,既不是电解质也不是非电解质;
⑧乙醇不能导电,属于非电解质;
⑨熔化的KNO3能导电,属于电解质;
⑩HCl不能导电.溶于水能导电,属于电解质;故答案为:①②⑦⑨;④⑤⑨⑩;③⑧.
点评 本题考查了电解质和非电解质的概念,难度不大,注意电解质和非电解质的区别.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
18.根据元素周期律,卤族元素的下列性质从上到下依次递增的有( )
| A. | 金属性 | B. | 非金属性 | C. | 原子半径 | D. | 单质的氧化性 |
19.设NA为阿伏加德罗常数的值.下列说法错误的是( )
| A. | 标准状况下,18 g H2O中含有的质子数为10 NA | |
| B. | 标准状况下,2.24 L Cl2通入水中,反应转移的电子数为0.1 NA | |
| C. | 常温常压下,53.5 g NH4Cl晶体中含有共价键的数目为4 NA | |
| D. | 常温常压下,2 L 0.5 mol•L-1 硫酸钾溶液中阴、阳离子总数大于3 NA |
16.下列有关垃圾处理的方法正确的是( )
| A. | 垃圾处理的方法只有卫生填埋和焚烧 | |
| B. | 将垃圾分类并回收利用是垃圾处理的发展方向 | |
| C. | 填埋垃圾不需要处理,只深埋即可 | |
| D. | 焚烧垃圾会产生大量污染空气的物质,故绝不宜采用此法 |
3.设NA表示阿伏加德罗常数的值,下列说法中正确的是( )
| A. | 1 mol NH4+ 所含质子数为10NA | |
| B. | 10克氖气所含原子数约为NA | |
| C. | 22.4 L SO2所含的分子数为NA | |
| D. | 2.3克金属钠变为钠离子时失去的电子数是0.1NA |
15.用H2O2溶液处理含NaCN的废水的反应原理为:NaCN+H2O2+H2O=NaHCO3+NH3,已知:HCN的酸性比H2CO3弱.下列有关说法正确的是( )
| A. | 该反应中氮元素被氧化 | |
| B. | 该反应中H2O2作还原剂 | |
| C. | 0.1mol•L-1NaCN溶液中含有HCN和CN-的总数为0.1×6.02×1023 | |
| D. | 实验室配制NaCN溶液时,需加入适量的NaOH溶液 |
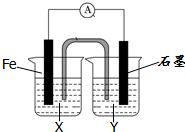 理论上任何一个自发的氧化还原反应均可以设计成原电池,根据氧化还原反应:Fe+2Fe3+=2Fe2+设计的原电池如图所示,其中盐桥内盛装有含KNO3饱和溶液的琼脂.
理论上任何一个自发的氧化还原反应均可以设计成原电池,根据氧化还原反应:Fe+2Fe3+=2Fe2+设计的原电池如图所示,其中盐桥内盛装有含KNO3饱和溶液的琼脂.