题目内容
5.HA为酸性略强于醋酸的一元弱酸,在等浓度的 NaA和HA的混合溶液中,离子浓度关系一定不正确的是( )| A. | c(Na+)+c(H+)=c(A-)+c(OH-) | B. | c(A-)>c(Na+)>c(H+)>c(OH-) | ||
| C. | 2c(Na+)=c(A-)+c(HA) | D. | c(Na+)>c(A-)>c(H+)>c(OH-) |
分析 HA为酸性略强于醋酸的一元弱酸,在等浓度的 NaA和HA的混合溶液中HA电离程度大于A-离子水解,溶液显酸性,
A.溶液中存在电荷守恒,溶液中阴阳离子所带电荷总数相同;
B.在等浓度的 NaA和HA的混合溶液中HA电离程度大于A-离子水解;
C.溶液中存在物料守恒分析;
D.在等浓度的 NaA和HA的混合溶液中HA电离程度大于A-离子水解.
解答 解:A.溶液中存在电荷守恒,c(Na+)+c(H+)=c(A-)+c(OH-),故A正确;
B.在等浓度的 NaA和HA的混合溶液中HA电离程度大于A-离子水解,溶液中离子浓度大小c(A-)>c(Na+)>c(H+)>c(OH-),故B正确;
C.在等浓度的 NaA和HA的混合溶液中存在物料守恒,2c(Na+)=c(A-)+c(HA),故C正确;
D.在等浓度的 NaA和HA的混合溶液中HA电离程度大于A-离子水解,溶液中离子浓度大小c(A-)>c(Na+)>c(H+)>c(OH-),故D错误;
故选D.
点评 本题考查了离子浓度大小比较,根据电解质的性质确定溶液酸碱性,根据溶液酸碱性再结合电荷守恒、物料守恒来分析解答,离子浓度大小常常与盐类水解、弱电解质电离联合考查,题目难度中等.

练习册系列答案
 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案
相关题目
12.有关卤素的说法正确的是( )
| A. | 卤素是典型的非金属元素,其单质只具有氧化性而无还原性 | |
| B. | 卤素单质的熔点随相对分子质量的增大而升高 | |
| C. | 卤化银都不溶于水,也不溶于稍硝酸 | |
| D. | 卤化氢的水溶液都是强酸 |
13.下列叙述正确的是( )
| A. | c( NH4+)相等的NH4Cl溶液和(NH4)2Fe( SO4)2溶液中:c(Cl-)>c( SO42-) | |
| B. | 常温下,将pH=5的H2S04溶液加水稀释1000倍,所得溶液的pH=8 | |
| C. | 0.2 mol/LCH3COOH溶液与0.1 mol/LNaOH溶液等体积混合所得的溶液中:c( CH3COOH)+c( CH3COO -)=2c(Na+)=0.2 mol/L | |
| D. | 用甲基橙作指示剂,用标准盐酸滴定未知浓度的氨水,至终点时,溶液中:c(NH4+)=c(Cl-) |
13.小明体检的血液化验单中,葡萄糖为 5.9mmol/L.表示该体检指标的物理量是( )
| A. | 溶解度(s ) | B. | 物质的量浓度(c ) | C. | 质量分数(w%) | D. | 摩尔质量(M ) |
20.有关溴乙烷的下列叙述中,正确的是( )
| A. | 溴乙烷不溶于水,能溶于大多数有机溶剂 | |
| B. | 溴乙烷与NaOH的醇溶液共热可生成乙醇 | |
| C. | 在溴乙烷中滴入AgNO3溶液,立即有淡黄色沉淀生成 | |
| D. | 溴乙烷通常用乙烷与液溴直接反应来制取 |
10.下列物质中含有Cl-的是( )
| A. | 氯水 | B. | 液氯 | C. | 次氯酸钠固体 | D. | 熔融的氯酸钾 |
17.碘晶体升华时,下列所述内容发生变化的是( )
| A. | 分子内共价键 | B. | 分子间的作用力 | ||
| C. | 分子间的距离 | D. | 分子内共价键的键长 |
15.在一定温度下,将气体X与气体Y各0.16mol充入10L恒容密闭容器中,发生反应:X(g)+Y(g)?2Z(g)△H<0,一段时间后达到平衡.反应过程中测定的数据如表:下列说法正确的是( )
| t∕min | 2 | 4 | 7 | 9 |
| n(Y)∕mol | 0.12 | 0.11 | 0.10 | 0.10 |
| A. | 反应前4min的平均反应速率υ(Z)=0.0125 mol•L-1•min-1 | |
| B. | 其他条件不变,降低温度,反应达到新平衡前υ(逆)>υ(正) | |
| C. | 该温度下此反应的平衡常数K=1.44 | |
| D. | 其他条件不变,再充入0.2molZ,达平衡时X的体积分数增大 |
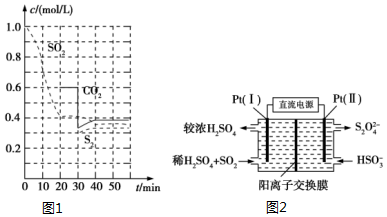 SO2直接排放会对环境造成危害.SO2的尾气处理通常有以下几种方法:
SO2直接排放会对环境造成危害.SO2的尾气处理通常有以下几种方法: