题目内容
下列关于能量的变化及反应热的说法中正确的是( )
| A、任何化学反应都有反应热 |
| B、有些化学键断裂时吸收能量,有些化学键断裂时放出能量 |
| C、新化学键的形成不一定放出能量 |
| D、有热量变化的反应一定有化学键的断裂与形成 |
考点:反应热和焓变
专题:化学反应中的能量变化
分析:A、化学反应的实在是反应物化学键断裂和生成物中化学键的形成,反应过程中一定伴随能量变化;
B、化学键断裂过程吸收能量;
C、形成新化学键一定放出能量;
D、有热量变化的反应不一定存在化学键的断裂与形成;
B、化学键断裂过程吸收能量;
C、形成新化学键一定放出能量;
D、有热量变化的反应不一定存在化学键的断裂与形成;
解答:
解:A、化学反应的实在是反应物化学键断裂和生成物中化学键的形成,过程中一定伴随能量变化,所以任何化学反应都有反应热,故A正确;
B、化学键断裂时是吸收能量,不能放出能量,故B错误;
C、化学反应的实在是反应物化学键断裂和生成物中化学键的形成,断裂化学键吸收能量,形成化学键放出能量,故C错误;
D、有热量变化的反应不一定有化学键的断裂与形成,如氢氧化钠溶解过程中化学键断裂,无化学键形成,冰雪融化放热无化学键变化,故D错误;
故选A.
B、化学键断裂时是吸收能量,不能放出能量,故B错误;
C、化学反应的实在是反应物化学键断裂和生成物中化学键的形成,断裂化学键吸收能量,形成化学键放出能量,故C错误;
D、有热量变化的反应不一定有化学键的断裂与形成,如氢氧化钠溶解过程中化学键断裂,无化学键形成,冰雪融化放热无化学键变化,故D错误;
故选A.
点评:本题考查了化学反应实质理解,能量变化分析判断,注意化学键的变化与能量的变化,题目较简单.

练习册系列答案
相关题目
由配位键形成的离子[Pt(NH3)6]2+和[PtCl4]2-中,两个中心离子铂的化合价是( )
| A、都是+8 | B、都是+6 |
| C、都是+4 | D、都是+2 |
下列事实不能用勒沙特列原理解释的是( )
| A、高压有利于合成氨的反应 |
| B、加入催化剂有利于合成氨的反应 |
| C、红棕色的NO2,加压后颜色先变深后变浅 |
| D、将混合气体中的氨气液化有利于合成氨反应 |
在t°C时,100g水中加入mgNa2CO3或加ngNa2CO3?10H2O,均可使溶液达到饱和,则m和n的关系式正确的是( )
A、m=
| ||
B、m=
| ||
C、m=
| ||
D、m=
|
已知1mol白磷变成红磷放出73.56 kJ?mol-1的热量,下列两个反应
P4(白磷7S)+5O2(g)=2P2O5(s)△H1
4P(红磷7S)+5O2(g)=2P2O5(s)△H2
△H1和△H2的关系正确的是( )
P4(白磷7S)+5O2(g)=2P2O5(s)△H1
4P(红磷7S)+5O2(g)=2P2O5(s)△H2
△H1和△H2的关系正确的是( )
| A、△H1=△H2<0 |
| B、△H1>△H2.>0 |
| C、△H1<△H2<0 |
| D、△H2<△H1<0 |
NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A、在常温下常压下,11.2 L氯气含有的分子数为0.5NA |
| B、在常温下常压下,1 mol氦气含有的分子数为2NA |
| C、32g氧气所含原子数目为2NA |
| D、在同温同压时,相同体积的任何气体单质所含的原子数目相同 |
关于氮的变化关系图如下:
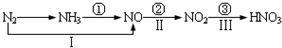
则下列说法不正确的是( )

则下列说法不正确的是( )
| A、路线①②③是工业生产硝酸的主要途径 |
| B、路线Ⅰ、Ⅱ、Ⅲ是雷电固氮生成硝酸的主要途径 |
| C、上述所有反应都是氧化还原反应 |
| D、氮气可在足量的氧气中通过一步反应生成NO2 |