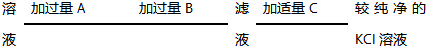题目内容
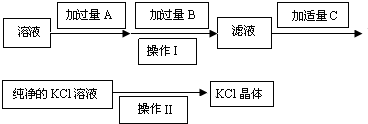
为了除去KCl溶液中少量的MgCl2、MgSO4,可选用Ba(OH)2、HCl和K2CO3三种试剂,按如图步骤操作:

(1)写出三种试剂的化学式:A
(2)加过量A的目的是:
(3)加过量B的目的是:

(1)写出三种试剂的化学式:A
Ba(OH)2
Ba(OH)2
,BK2CO3
K2CO3
,CHCl
HCl
.(2)加过量A的目的是:
为了除尽Mg2+和SO42-
为了除尽Mg2+和SO42-
,有关反应的化学方程式为:MgCl2+Ba(OH)2═Mg(OH)2↓+BaCl2
MgCl2+Ba(OH)2═Mg(OH)2↓+BaCl2
、MgSO4+Ba(OH)2═BaSO4↓+Mg(OH)2↓
MgSO4+Ba(OH)2═BaSO4↓+Mg(OH)2↓
.(3)加过量B的目的是:
为了除尽过量的Ba2+
为了除尽过量的Ba2+
,有关反应的离子反应方程式为:CO32-+Ba2+═BaCO3↓
CO32-+Ba2+═BaCO3↓
.分析:分析混合物的组成特点,根据提纯流程,选择所提供的试剂逐步提纯氯化钾,Ba(OH)2可同时沉淀掉Mg2+、SO42-离子;反应生成的BaCl2和过量的Ba(OH)2可加入所选试剂中的K2CO3而除去;最后通过滴加盐酸可把过量的K2CO3及反应生成的KOH同时反应掉.
解答:解:(1)除去KCl溶液中的少量MgCl2和MgSO4,可看成把Mg2+、SO42-沉淀而除去,因此选择所提供试剂中的Ba(OH)2可同时沉淀掉Mg2+、SO42-离子;反应生成的BaCl2和过量的Ba(OH)2可加入所选试剂中的K2CO3而除去;最后通过滴加盐酸可把过量的K2CO3及反应生成的KOH同时反应掉而生成KCl;
故答案为:Ba(OH)2;K2CO3;HCl.
(2)为确保混合溶液中的MgCl2和MgSO4全部反应而沉淀掉,故应加入过量的Ba(OH)2,生成Mg(OH)2、BaSO4,即MgCl2+Ba(OH)2═Mg(OH)2↓+BaCl2、MgSO4+Ba(OH)2═BaSO4↓+Mg(OH)2↓;
故答案为:为了除尽Mg2+和SO42-;MgCl2+Ba(OH)2═Mg(OH)2↓+BaCl2、MgSO4+Ba(OH)2═BaSO4↓+Mg(OH)2↓;
(3)为确保溶液是的Ba2+全部沉淀而除去,应加入过量的Ba(OH)2到沉淀不再产生;反应生成碳酸钡沉淀、氢氧化钾,反应方程式为K2CO3+Ba(OH)2═BaCO3↓+2KOH;
故答案为:为了除尽过量的Ba2+;CO32-+Ba2+═BaCO3↓.
故答案为:Ba(OH)2;K2CO3;HCl.
(2)为确保混合溶液中的MgCl2和MgSO4全部反应而沉淀掉,故应加入过量的Ba(OH)2,生成Mg(OH)2、BaSO4,即MgCl2+Ba(OH)2═Mg(OH)2↓+BaCl2、MgSO4+Ba(OH)2═BaSO4↓+Mg(OH)2↓;
故答案为:为了除尽Mg2+和SO42-;MgCl2+Ba(OH)2═Mg(OH)2↓+BaCl2、MgSO4+Ba(OH)2═BaSO4↓+Mg(OH)2↓;
(3)为确保溶液是的Ba2+全部沉淀而除去,应加入过量的Ba(OH)2到沉淀不再产生;反应生成碳酸钡沉淀、氢氧化钾,反应方程式为K2CO3+Ba(OH)2═BaCO3↓+2KOH;
故答案为:为了除尽过量的Ba2+;CO32-+Ba2+═BaCO3↓.
点评:这类题的关键是除杂不能引入新杂质,如果前面的操作带入杂质不可避免,那么一定要在后续操作中除掉杂质.在这一题中就是要让碳酸根除去过量的钡离子(前面为了除去硫酸根离子).

练习册系列答案
 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案
相关题目
(11分)为了除去KCl溶液中少量的MgCl2、MgSO4,可选用Ba(OH)2、HCl和K2CO3三种试剂,按下图步骤操作:
| 溶液 | 加过量A | 加过量B | 滤液 | 加适量C | 较纯净的KCl溶液 |
|
|
|
|
(1)写出三种试剂的化学式:A ,B ,C 。
(2)加过量A的原因是: ,
有关反应的化学方程式为:
(3)加过量B的原因是: ,
有关反应的化学方程式为: