题目内容
铝在自然界中主要以铝矾土(Al2O3.xH2O)氧化物的形式存在.镓(Ga)常以极少量分散于铝矿中.铝和镓的性质相似,如氢氧化物都是难溶的两性氢氧化物.工业上提取铝是以铝矾土为原料,用NaOH溶液处理铝矿,生成NaAlO2和NaGaO2;然后通入CO2,得Al(OH)3沉淀,而NaGaO2留在溶液中(循环多次后成为提取镓的原料);过滤,将沉淀干燥、灼烧得到Al2O3;最后将Al2O3在一定条件下高温电解,在阴极上得到熔融的金属铝,纯度可达99%左右,放出后铸成铝锭.
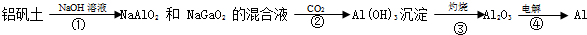
(1)写出各步反应的化学方程式:
①
②
③
④
(2)在NaAlO2和NaGaO2的混合液中通入CO2,只有Al(OH)3沉淀,而没有Ga(OH)3沉淀的原因可能是
.
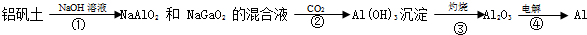
(1)写出各步反应的化学方程式:
①
②
③
④
(2)在NaAlO2和NaGaO2的混合液中通入CO2,只有Al(OH)3沉淀,而没有Ga(OH)3沉淀的原因可能是
考点:金属冶炼的一般原理,物质的分离、提纯的基本方法选择与应用
专题:元素及其化合物
分析:根据已知信息:铝和镓的性质相似,氢氧化物都是难溶的两性氢氧化物,根据金属铝以及氢氧化铝、氧化铝的性质来书写方程式.
解答:
解:(1)①氧化铝和氧化镓都可以和氢氧化钠之间发生反应,其反应原理为:Al2O3+2NaOH=2NaAlO2+H2O 和Ga2O3+2NaOH═2NaGaO2+H2O,
故答案为:Al2O3+2NaOH=2NaAlO2+H2O 和Ga2O3+2NaOH═2NaGaO2+H2O;
②向偏铝酸钠中通入二氧化碳会发生反应生成氢氧化铝和碳酸钠,即2NaAlO2+CO2+2H2O═2Al(OH)3↓+Na2CO3,
故答案为:2NaAlO2+CO2+2H2O═2Al(OH)3↓+Na2CO3;
③氢氧化铝受热易分解:2Al(OH)3
Al2O3+3H2O,故答案为:2Al(OH)3
Al2O3+3H2O;
④电解熔融的氧化铝可以获得金属铝合氧气,即2Al2O3
4Al+3O2↑,故答案为:2Al2O3
4Al+3O2↑;
(2)化学反应遵循强酸制弱酸的原理,在NaAlO2和NaGaO2的混合液中通入CO2,只有Al(OH)3沉淀,而没有Ga(OH)3沉淀,可能是镓酸酸性强于碳酸,故答案为:镓酸酸性强于碳酸.
故答案为:Al2O3+2NaOH=2NaAlO2+H2O 和Ga2O3+2NaOH═2NaGaO2+H2O;
②向偏铝酸钠中通入二氧化碳会发生反应生成氢氧化铝和碳酸钠,即2NaAlO2+CO2+2H2O═2Al(OH)3↓+Na2CO3,
故答案为:2NaAlO2+CO2+2H2O═2Al(OH)3↓+Na2CO3;
③氢氧化铝受热易分解:2Al(OH)3
| ||
| ||
④电解熔融的氧化铝可以获得金属铝合氧气,即2Al2O3
| ||
| ||
(2)化学反应遵循强酸制弱酸的原理,在NaAlO2和NaGaO2的混合液中通入CO2,只有Al(OH)3沉淀,而没有Ga(OH)3沉淀,可能是镓酸酸性强于碳酸,故答案为:镓酸酸性强于碳酸.
点评:本题是一道信息迁移题,考查学生金属铝以及化合物的性质、化学方程式的书写等,难度不大.

练习册系列答案
相关题目
已知2SO2+O2?2SO3为放热反应,对该反应的下列说法正确的是( )
| A、O2的能量一定高于SO2的能量 |
| B、2molSO2和1molO2的总能量一定高于2molSO3的总能量 |
| C、SO2的能量一定高于SO3的能量 |
| D、因该反应为放热反应,故不必加热就可发生 |
25℃时,下列说法中,不正确的是( )
| A、将体积均为100mL、浓度均为0.1mol/L的Ba(OH)2溶液与Na2SO4溶液混合,若混合后溶液的体积为100mL,则所得溶液的pH=13 |
| B、将等体积等浓度的醋酸与CH3COONa溶液混合,所得溶液中:c(Na+)+c(H+)═c(CH3COO-)+c(OH-) |
| C、将等体积等浓度的Na2CO3溶液与NaHCO3溶液混合,所得溶液中:2c(Na+)═c(CO32-)+c(HCO3-)+c(H2CO3) |
| D、将等体积等浓度的Na2CO3溶液与NaOH溶液混合,所得溶液中:c(Na+)>c(OH-)>c(CO32-)>c(H+) |
下列实验操作或装置符合实验要求的是( )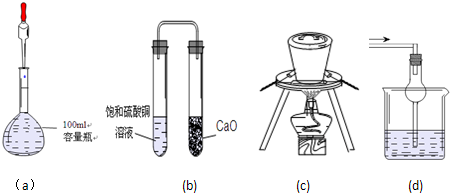

| A、(a) 可用于定容并量取15.00 mL NaOH溶液 |
| B、(b)装置放置一段时间后,饱和CuSO4溶液中出现蓝色晶体 |
| C、(c)可用于高温煅烧石灰石 |
| D、(d)可用于易溶于水的尾气吸收 |
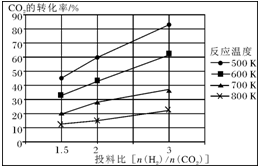 燃煤废气中的氮氧化物(NOx)、二氧化碳等气体,常用下列方法处理,以实现节能减排、废物利用等.
燃煤废气中的氮氧化物(NOx)、二氧化碳等气体,常用下列方法处理,以实现节能减排、废物利用等. 水煤气(CO 和H2)是重要燃料和化工原料,可用水蒸气通过炽热的炭层制得:
水煤气(CO 和H2)是重要燃料和化工原料,可用水蒸气通过炽热的炭层制得: 如图中各物质均由常见元素(原子序数≤20)组成.已知A、B、K为单质,且在常温下A和K为气体,B为固体.D为常见的无色液体.I是一种常用的化肥,在其水溶液中滴加AgNO3溶液有不溶于稀HNO3的白色沉淀产生.J是一种实验室常用的干燥剂.它们的相互转化关系如图所示(图中反应条件未列出).
如图中各物质均由常见元素(原子序数≤20)组成.已知A、B、K为单质,且在常温下A和K为气体,B为固体.D为常见的无色液体.I是一种常用的化肥,在其水溶液中滴加AgNO3溶液有不溶于稀HNO3的白色沉淀产生.J是一种实验室常用的干燥剂.它们的相互转化关系如图所示(图中反应条件未列出).