题目内容
7.以乙烯为原料合成化合物C的流程如图所示: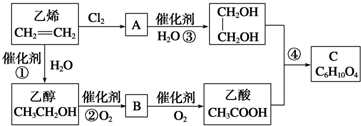
(1)C中官能团名称为酯基,①的反应类型为加成反应.
(2)写出A的同分异构体的结构简式:CH3CHCl2.
(3)写出反应③的产物与足量金属钠反应的化学方程式:HOCH2CH2OH+2Na→NaOCH2CH2ONa+H2↑.
(4)写出反应④的化学方程式:HOCH2CH2OH+2CH3COOH$?_{△}^{浓硫酸}$CH3COOCH2CH2OOCCH+2H2O.
分析 乙烯和氯气发生加成反应生成A,A为CH2ClCH2Cl,A发生水解反应生成HOCH2CH2OH,乙烯和水发生加成反应生成乙醇,乙醇发生催化氧化反应生成B,B为CH3CHO,B发生氧化反应生成CH3COOH,HOCH2CH2OH和CH3COOH发生酯化反应生成C,根据C分子式知,C结构简式为CH3COOCH2CH2OOCCH3,据此分析解答.
解答 解:乙烯和氯气发生加成反应生成A,A为CH2ClCH2Cl,A发生水解反应生成HOCH2CH2OH,乙烯和水发生加成反应生成乙醇,乙醇发生催化氧化反应生成B,B为CH3CHO,B发生氧化反应生成CH3COOH,HOCH2CH2OH和CH3COOH发生酯化反应生成C,根据C分子式知,C结构简式为CH3COOCH2CH2OOCCH3,
(1)C结构简式为CH3COOCH2CH2OOCCH3,C中官能团名称为酯基,①的反应类型为 加成反应,故答案为:酯基;加成反应;
(2)A的同分异构体的结构简式CH3CHCl2,故答案为:CH3CHCl2;
(3)反应③的产物与足量金属钠反应的化学方程式为HOCH2CH2OH+2Na→NaOCH2CH2ONa+H2↑,故答案为:HOCH2CH2OH+2Na→NaOCH2CH2ONa+H2↑;
(4)④为乙二醇与乙酸在浓硫酸条件下发生酯化反应,化学方程式为:HOCH2CH2OH+2CH3COOH$?_{△}^{浓硫酸}$CH3COOCH2CH2OOCCH+2H2O,
故答案为:HOCH2CH2OH+2CH3COOH$?_{△}^{浓硫酸}$CH3COOCH2CH2OOCCH+2H2O.
点评 本题考查有机物推断,为高频考点,侧重考查学生分析推断能力,明确官能团及其性质关系是解本题关键,熟练掌握常见有机反应类型、有机物官能团及其性质,题目难度不大.

 黄冈课堂作业本系列答案
黄冈课堂作业本系列答案 单元加期末复习先锋大考卷系列答案
单元加期末复习先锋大考卷系列答案| A. | m+n<p | B. | 平衡向逆反应方向移动 | ||
| C. | C的体积分数增大 | D. | A的转化率降低 |
①元素的种类 ②如果在水溶液中反应,反应前与反应后阳离子所带的正电荷总数
③分子的数目 ④原子的数目 ⑤反应前物质的质量总和与反应后物质的质量总和.
| A. | ①③④ | B. | ②③⑤ | C. | ①④⑤ | D. | ②④⑤ |
| A. | 该混盐具有较强的氧化性 | |
| B. | 该混盐中氯元素的化合价为+1和-1价 | |
| C. | 该混盐与盐酸反应产生1mol Cl2时转移1mol电子 | |
| D. | 该混盐的水溶液显酸性 |
| A. | 澄清透明的无色溶液:MnO4- Na+ I- Mg2+ | |
| B. | 含有0.1mol/L Fe3+ 的溶液中:Na+ Ca2+ SCN- SO42- | |
| C. | 与铝片反应产生氢气的溶液:CO32- SO42- Na+ NH4+ | |
| D. | 使酚酞溶液变红的溶液:Na+ Cl- NO3- Ba2+ |
| A. | 在空气中敞口久置的浓硫酸,溶液质量增大(难挥发性) | |
| B. | 在加热条件下铜与浓硫酸反应(强氧化性、酸性) | |
| C. | 蔗糖与浓硫酸反应中有海绵状的炭生成(吸水性) | |
| D. | 浓硫酸与少量胆矾晶体混合,晶体由蓝色变成白色(脱水性) |
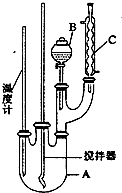 实验室制备硝基苯的反应原理和实验装置如下:
实验室制备硝基苯的反应原理和实验装置如下: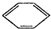 +HO-NO2$→_{50-60℃}^{H_{2}SO_{4}}$
+HO-NO2$→_{50-60℃}^{H_{2}SO_{4}}$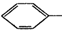 NO2+H2O△H<0
NO2+H2O△H<0反应中存在的主要副反应有:在温度稍高的情况下会生成间二硝基苯.
有关数据列如下表:
| 物质 | 熔点/℃ | 沸点/℃ | 密度/g•cm-3 | 溶解性 |
| 苯 | 5.5 | 80 | 0.88 | 微溶于水 |
| 硝基苯 | 5.7 | 210.9 | 1.205 | 难溶于水 |
| 间二销基苯 | 89 | 301 | 1.57 | 微溶于水 |
| 浓硝酸 | 83 | 1.4 | 易溶于 | |
| 浓硫酸 | 338 | 1.84 | 易溶于水 |
回答下列问题:
(1)图中装置C的作用是冷凝回流.
(2)配制混合酸时,能否将浓硝酸加入到浓硫酸中,说明理由:不能,容易发生迸溅.
(3)为了使反应在50℃~60℃下进行,常用的方法是水浴加热.反应结束并冷却至室温后A中液体就是粗硝基苯,粗硝基苯呈黄色的原因是溶有浓硝酸分解产生的NO2(或硝酸)等杂质.
(4)在洗涤操作中,第二次水洗的作用是洗去残留的NaOH及生成的盐.
(5)在蒸馏纯化过程中,因硝基苯的沸点高于140℃,应选用空气冷凝管,不选用水直形冷凝管的原因是以免直形冷凝管通水冷却时导致温差过大而发生炸裂.
(6)本实验所得到的硝基苯产率是72%.
| A. | 金属表面的氧化膜都很致密,能对金属起到保护作用 | |
| B. | 金属表面的氧化膜的形成都需要金属暴露在空气中很长时间才会形成 | |
| C. | 金属表面的氧化膜薄层的厚度会随着金属暴露在空气中的时间增长而加厚 | |
| D. | 某些金属表面氧化膜的形成对这些金属的广泛应用起到关键作用 |
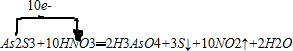 ;
;